Термин «грыжа» подразумевает выход органа или его части за пределы анатомического расположения через патологическое или физиологическое отверстие под кожу, в мышечное пространство или в соседние анатомические полости. После оперативного лечения паховой грыжи наступает период реабилитации. От правильности подбора восстановительных методик зависит скорость возвращения пациента к привычной жизни.
По анатомическим признакам грыжи делятся на внутренние и наружные.
Внутренние грыжи, в свою очередь, разделяются на диафрагмальные и внутрибрюшные.
Диафрагмальные грыжи образуются вследствие выхода органов брюшной полости в грудной отдел через патологические или естественные дефекты диафрагмы.
Внутрибрюшные грыжи образуются из-за попадания органа или его части в карманы брюшины.
Чаще встречаются наружные грыжи – выхождение органа или его части из области его анатомического расположения через искусственные или естественные отверстия с пристеночным листком брюшины.
От грыжи необходимо отличать выпадение (эвентрацию) органа – это выпячивание органа наружу через дефект брюшной стенки. Как правило, причиной эвентрации является нарушение целостности брюшины вследствие ее травмы (ранения и др.). Другими словами, эта патология предполагает наличие грыжевого мешка (париетального листка брюшины), которого нет при эвентрации.
По анатомической локализации выделяют следующие виды грыж:
- пупочная;
- паховая;
- бедренная;
- мечевидного отростка;
- белой линии живота (в т. ч. эпигастральная);
- дугообразной линии;
- боковая (спигелиевой или полулунной линии);
- поясничная (треугольника Пти, ромба Грифельда-Лесгафта);
- запирательная;
- промежностная;
- седалищная.
Паховая грыжа относится к нарушениям брюшной стенки. Это патологическое выпячивание брюшины с внутренними органами в пространство пахового канала.
Паховый канал представляет собой туннель длиной в 4-6 см, в котором у женщин проходят круглые связки матки, а у мужчин семенные канатики. Этот отдел расположен в нижней паховой области. В случае неплотного прилегания мышц к семенному канатику или связкам матки в данной области образуется паховый промежуток, который является важным звеном в формировании паховой грыжи.
- прямые и косые паховые грыжи;
- врожденные и приобретенные;
- ущемленные и вправимые (неущемленные);
- односторонние и двусторонние.
Врожденную грыжу можно исправить только хирургическим путем. При появлении патологии у взрослых есть возможность лечиться консервативно или оперативно в зависимости от наличия показаний и противопоказаний к первому или второму методу.
Консервативное лечение сводится к ношению специального бандажа, возвращающего грыжевое содержимое на анатомическое место и защищающего пациента от защемления грыжевого мешка. Такая терапия назначается по определенным показаниям, т. к. не способна избавить пациента от заболевания, а только облегчает состояние. К тому же длительное ношение бандажа провоцирует развитие атрофии мышц брюшной стенки и усугубление патологии.
Оперативные методики лечения грыжи бывают двух видов: путем открытого доступа или лапароскопические.
- Наличие противопоказаний к хирургическому лечению у детей и взрослых.
- Рецидив заболевания (грыжи) после оперативного вмешательства.
- Наличие у пациента объемной грыжи, требующей нескольких операций. Бандаж используют во временной промежуток между хирургическими вмешательствами.
- Наличие неосложненной грыжи является показанием для плановой операции.
- Ущемление грыжевого мешка требует экстренного хирургического вмешательства.
- Рецидивирующие грыжи.
- Послеоперационные грыжи.
- Развитие спаечного процесса.
- Объемные грыжи у пожилых пациентов (старше 70 лет) с сопутствующими декомпенсированными заболеваниями дыхательной или сердечно-сосудистой системы.
- Беременность.
- Цирроз печени с портальной гипертензией.
- Увеличение селезенки.
- Тяжелая почечная недостаточность.
- Варикозное расширение вен пищевода и толстого кишечника.
- Декомпенсация сахарного диабета.
Операционные:
- Повреждение внутренних органов (стенок мочевого пузыря, кишечника).
- Нарушение целостности сосудов.
- Повреждение нервов (подвздошно-подчревного и подвздошно-пахового) в послеоперационном периоде является причиной появления выраженного болевого синдрома, а позднее за счет атрофии мышц может спровоцировать возникновение рецидива заболевания.
- Деформация семенного канатика у мужчин.
- Иссечение семявыносящих протоков у мужчин с развитием аспермии.
В раннем послеоперационном периоде:
- Нагноение раны.
- Лигатурные свищи.
- Гематомы в области раны.
- Серомы.
- Нарушение трофики яичек и стойкий отек мошонки как следствие сдавления семенного канатика при пластике пахового канала.
В позднем послеоперационном периоде:
- Рецидив грыжи.
- Нарушение сперматогенной и гормональной функции яичек или секреторной функции предстательной железы со снижением половой и детородной функций.
После оперативного лечения следует период реабилитации. От правильности построения методик восстановления организма зависит самочувствие пациента и скорость возвращения к привычной для него бытовой и трудовой жизни.
Ходить больному можно сразу после операции, а при проведении хирургических манипуляций под спинальной анестезией – спустя 3 часа, но при отсутствии противопоказаний, с разрешения хирурга и реабилитолога.
При проведении плановой операции без осложнений под местной анестезией пациент может выписаться через 2-3 часа.
В течение 2 недель после манипуляции необходимо ограничить подъем тяжестей до 5 кг, а через месяц уже можно вернуться к обычной активности.
Если пластика была выполнена собственными тканями, сроки реабилитации удлиняются до 2-3 месяцев.
Показанием для назначения лечебной физкультуры является подготовка к операции и реабилитация после нее.
В ранний послеоперационный период (до снятия швов) задачами лечебной физкультуры являются:
- профилактика спаечного процесса;
- предупреждение осложнений;
- формирование эластичного рубца;
- улучшение работы сердечно-сосудистой и дыхательной систем;
- стабилизация психоэмоционального состояния пациента.
В предоперационный период:
- нестабильное состояние пациента;
- гипертермия (более 38°С);
- ущемление грыжи;
- опасность кровотечения;
- выраженный болевой синдром.
- тяжелое состояние пациента;
- острая сердечно-сосудистая недостаточность;
- развитие перитонита.
При отсутствии противопоказаний лечебная физкультура назначается уже с первых часов после окончания операции.
Сначала выполняются комплексы дыхательной гимнастики, затем к ним добавляют упражнения для конечностей.
После обширных операций в первые несколько суток пациенту может быть назначен постельный режим. В этом случае лечебная гимнастика выполняется лежа на кровати. После разрешения хирурга и врача-реабилитолога исходное положение меняется на полусидячее и сидячее.
В лежачем положении делаются упражнения для дыхательной и сердечно-сосудистой систем, для верхних и нижних конечностей как динамические, так и статические. Затем добавляется легкая гимнастика для мышц брюшного пресса, далее включаются повороты корпуса, а для глубоких мышц промежности практикуется чередование сокращения и расслабления.
Обязательно стоит помнить о том, что в этот период необходимо использовать бандаж для предотвращения развития послеоперационных осложнений.
Задачи лечебной физкультуры в позднем послеоперационном периоде (до 2—3-й недели):
- стабилизация гомеостаза (внутреннего равновесия в организме);
- ускорение процесса регенерации тканей в области операции;
- возвращение пациента к привычной бытовой и трудовой активности;
- расширение режима двигательной активности;
- увеличение толерантности к физической нагрузке;
- профилактика нарушения осанки.
В данный период назначаются упражнения с дополнительным гимнастическим оборудованием: мячами, палками, у гимнастической стенки и т. д., выполняются двигательные комплексы для всех суставов и групп мышц.
Задачи лечебной физкультуры в отдаленном послеоперационном периоде (через 3 недели после операции до восстановления работоспособности пациента):
- тренировка сердечно-сосудистой и дыхательной систем организма;
- адаптация к возрастающей физической нагрузке;
- восстановление трудоспособности пациента.
В этот период используются комплексы лечебной гимнастики, направленные на общее укрепление организма, а также на тренировку мышц брюшного пресса, пешеходные прогулки, щадящие спортивные игры, ходьба на лыжах.
Помимо ЛФК в послеоперационном периоде необходимо назначать массаж с целью профилактики послеоперационных осложнений, связанных с гиподинамией (пневмония у ослабленных лиц, атрофия мышц).
Массаж проводится сегментарный на позвоночнике, а также на области живота для профилактики атонии кишечника и заканчивается в области нижних конечностей.
При образовании инфильтрата или флегмоны в области операции назначается УВЧ и лазеротерапия через чистую повязку.
Во время перевязки проводится ультрафиолетовое облучение раны и окружающих тканей.
При образовании спаек в брюшной полости и для восстановления нормального тонуса кишечника назначаются: сантиметровая терапия, диадинамотерапия, индуктотермия, лазеротерапия, а также грязе-, парафино- и озокеритолечение.
Пациенту необходимо помнить о важности точного выполнения рекомендаций и указаний врачей для благополучного восстановления после оперативного лечения паховой грыжи.
Хирургическое вмешательство часто становится единственным эффективным способом лечения, это касается и такой проблемы, как паховая грыжа, операция в данном случае спасает от тяжелых осложнений. Сегодня широко применяются различные методики, выбор которых зависит от состояния организма конкретного пациента и типа паховой грыжи (ПГ) у него.
Любая операция на паховой грыже подразумевает выполнение нескольких основных этапов:
- Формируется доступ к проблемной зоне – делается косой разрез
- Выделяют и удаляют грыжевой мешок
- Ушивают глубокое кольцо
- Производят пластику.
Такое оперирование позволяет добиться закрытия грыжевых ворот и устранения самой причины возникновения ПГ.
Еще до появления сетчатых имплантов, которые используются в операции при паховых грыжах, проводилась натяжная герниопластика. Вмешательства данного типа отличаются тем, что грыжевой мешок вправлялся обратно в брюшную полость, а ворота ПГ закрывались собственными окружающими тканями (мышцами и фасциями). Однако их приходилось подтягивать к грыжевым воротам, а это неизменно сопровождается травматизацией и нарушением кровообращения. Поэтому со временем эти ткани часто истончаются, швы прорезываются, стенка пахового канала вновь становится слабой и пропускает части органов.
В связи с этим такая операция при паховой грыже, как натяжная герниопластика, в 30 % случаев заканчивалась рецидивами. После нее возможно также появление осложнений. Сегодня эта методика уходит в прошлое и применяется все реже. Иногда ПГ устраняют данным способом в маленьких клиниках, где нет возможности использовать импланты.
Пациенты, которым предстоит подобная операция паховой грыжи, должны понимать, что риск повторного появления выпячивания остается довольно высоким. Кроме того, болезненные ощущения в послеоперационный период бывают выраженными и продолжительными.
Сегодня популярна аллопластика паховой грыжи. Она подразумевает применение сетчатых металлических имплантов.
Одной из них является пластика по Лихтенштейну. Основной ее принцип – сшивание тканей без натяжения. Это позволяет добиться минимальных кровопотерь и существенно снизить операционный травматизм, избежав тем самым развития осложнений. Укрепление стенки пахового канала осуществляется путем наложения специальной полимерной сетки, как показано на видео.
Сегодня используются безопасные, нетоксичные импланты, которые не вызывают аллергических и воспалительных реакций практически у всех пациентов. Через некоторое время они врастают в ткани, поэтому получившийся прочный каркас эффективно удерживает органы брюшной полости на месте. Существует несколько видов сеток, которые отличатся по своему составу. Хирург подбирает их для каждого пациента индивидуально. При крупной ПГ применяется сетка, которая рассасывается после ее прорастания соединительной тканью. Сетки из растворяющихся полимеров одновременно стимулируют процессы регенерации.
Иногда хирурги делают операцию с использованием имплантов, которые похожи на катушку. Они позволяют закрыть грыжевые ворота изнутри и снаружи, а также заполнить их. Это исключает возможность смешения сетки и рецидива ПГ. Для фиксации такого импланта требуется всего несколько узловых швов, поэтому боли в послеоперационном периоде практически нет. Сегодня активно внедряются импланты с нитиноловой рамкой, которая сохраняет форму сетки и максимально облегчает ее установку. Прибегать к фиксации таких имплантов швами не приходится, поэтому боль в послеоперационном периоде практически отсутствует. Ненатяжная герниопластика с применением сетчатых имплантов заканчивается рецидивами примерно в 1-3 % случаев, что считается довольно хорошим результатом.
Таким образом, пластика ПГ с помощью сетчатых имплантов имеет целый ряд преимуществ перед натяжным грыжесечением, и это подтверждают многочисленные положительные отзывы. Однако мальчики, у которых имеется врожденная пахово-мошоночная грыжа, оперируются несколько иначе. В частности, у детей не используются импланты.
Лапароскопическая герниопластика паховой грыжи проводится сегодня все чаще, однако не так широко, поскольку оборудование для осуществления таких операций имеется пока далеко не во всех клиниках. Очевидным преимуществом этой техники является минимальный операционный травматизм, так как доступ к грыжевому мешку осуществляется через маленькие проколы в брюшной стенке. Это дает возможность избежать различных осложнений и добиться прекрасного косметического эффекта.
Таким способом проводится не только операция на паховую грыжу, одновременно можно производить вмешательства на других органах брюшной полости. Грыжевой мешок также удаляется, помещается сетчатый имплант.
Большая продолжительность по сравнению с открытой ненатяжной герниопластикой – это недостаток, который имеет лапароскопическая операция на паховую грыжу. Кроме того, такие хирургические вмешательства проводятся только под общим наркозом, а это может быть противопоказанием для некоторых пациентов.
Однако после эндоскопической герниопластики боли в послеоперационном периоде менее интенсивные и продолжительные. Следует учитывать, что лапароскопия проводится только специально обученными хирургами при помощи эндоскопического оборудования.
Современные методы хирургического удаления ПГ позволяют не только снизить вероятность рецидивов, но также избавить пациента от болезненных ощущений. Если ранее после перенесенной натяжной герниопластики больной находился стационаре около недели, а нетрудоспособным оставался на протяжении месяца, то сейчас после того, как была проведена обтурационная герниопластика или герниопластика по Лихтенштейну, пациенты могут быть выписаны спустя сутки, уменьшается также срок их нетрудоспособности. Эндоскопическая герниопластика требует нахождения пациента в стационаре на протяжении 2-3 суток.
Всем больным требуется предоперационная подготовка. Это значит, что за несколько дней до того, как вырезают ПГ, следует отказаться от обильных ужинов после 18 часов. Также делается очистительная клизма, в день операции врачи обычно не рекомендуют есть и пить. В послеоперационном периоде дискомфорт в области шва сохраняется около двух суток. Через неделю пациенты возвращаются для удаления шовного материала, а также на повторный осмотр. Врач убеждается в том, что все удалось эффективно прооперировать, и осложнения не появились.
В редких случаях наблюдается патологическое скопление серозной жидкости в тканях передней стенки брюшной полости. Однако если серома обнаружена вовремя, ее легко ликвидировать. Для этого производится пункция под контролем ультразвукового исследования. Уже через несколько дней прооперированные пациенты возвращаются к своему нормальному образу жизни. Однако следует избегать тяжелых физических нагрузок в течение последующих двух недель, а лучше беречься от них весь месяц после того, как была сделана операция по паховой грыже.
Безусловно, существуют и другие осложнения, о которых пациентам следует знать. Их наличие во многом зависит от опыта и мастерства врача. В паховом канале у мужчин проходит семенной канатик, а также важные сосуды. Задача хирурга сводится к тщательному их выделению. Грыжесечение по методу Лихтенштейна сопряжено с риском повреждения многочисленных нервов. Иногда рубцово-спаечные процессы начинаются в месте, где семенной канатик проходит через имплант. Это может привести к нарушению кровообращения в яичке.
У женщин в случае пересечения круглой связки может произойти смещение матки. Наконец, всегда остается минимальная вероятность развития раневых осложнений, таких как гематомы, нагноения и инфильтраты. К счастью, такие случаи сегодня – большая редкость, и практически все операции по поводу ПГ заканчиваются благополучно. В послеоперационном периоде следует выполнять специальную легкую гимнастику, которая поможет укрепить переднюю брюшную стенку и избежать повторного появления ПГ. Кроме того, людям с избыточным весом крайне желательно избавиться от лишних килограммов.
Возникновение паховой грыжи сопровождается не только визуальным дефектом в результате выпячивания внутренних органов, но и внутренним дискомфортом и неприятными ощущениями. Увеличение давления на брюшную стенку, слабость соединительных тканей и патологические изменения в организме могут стать причиной возникновения грыжи. Заболеванию подвержены как дети, так и взрослые. У младенцев паховая грыжа зачастую имеет врожденный характер, у взрослых является следствием неправильного образа жизни и физиологической предрасположенности. Согласно исследованиям, паховое выпячивание чаще диагностируется у мужчин, у женщин грыжа может проявиться во время беременности и после родов.
Паховая грыжа требует хирургического лечения, консервативные методы способны лишь снять основную симптоматику и временно улучшить самочувствие больного. При возникновении выпячивания, необходимо сразу же обратиться к врачу и пройти комплексное обследование. Первым делом пациенту назначается рентгенологическое исследование, чтобы выявить размеры образования и его локализацию. Кроме того, проводится ультразвуковое исследование органов брюшной полости, чтобы исключить возможность ущемления и определить содержимое грыжевого мешка.
Первичная пальпация проводится в положении стоя и лежа. Осмотрев грыжу, врач определит возможность ее вправления и размеры грыжевых ворот. Если выпячивание достигло больших размеров, грыжа становится невправляемой и есть риск ущемления.
Перед проведением плановой операции больному необходимо сдать общий и биохимический анализ крови и мочу. Пациенту делают электрокардиограмму, может понадобиться дополнительная консультации гастроэнтеролога. Перед хирургическим вмешательством проводится анкетирование больного, где ему следует указать индивидуальную переносимость лекарств и наличие хронических заболеваний.
Если пациент имеет такую вредную привычку, как курение, за несколько дней до операции необходимо максимально снизить употребление никотина. Последний прием пищи и воды должен быть не меньше, чем за восемь часов до начала операции.
Исходя из сложности предстоящей операции и размеров грыжи, больному проводится грыжесечение. Существует несколько способов проведения хирургической манипуляции:
- открытый (с рассечением тканей);
- лапароскопия.
Операцию делают под местным или общим наркозом. При нормальном течении заболевания и отсутствии противопоказаний, а также детям — делают местный наркоз. Если пациент находится в шоковом состоянии перед предстоящим хирургическим вмешательством, манипуляция проводится под общим наркозом.
Во время проведения операции открытым способом, хирург делает надрез в области образования грыжи параллельно паховой связки. После этого рассекается грыжевой мешок и проводится осмотр внутренних органов, которые в него сместились. Если не произошло ущемление и некроза тканей, органы помещаются на свои места, а мешок отсекается. В случает осложнений, грыжевой мешок удаляется вместе с содержимым.
В процессе сшивания пахового канала, рана затягивается собственными тканями апоневроза или закрывается специальной синтетической сеткой. Использование сетчатого импланта имеет несколько неоспоримых преимуществ, в частности, отсутствие риска рецидива заболевания и расхождения швов.
Среди недостатков этого метода:
- длительный реабилитационный период;
- наличие послеоперационного рубца;
- возможность рецидива (если не используется полипропиленовая сетка).
В среднем, операция длится полтора-два часа, в зависимости от сложности выпячивания и опытности самого врача.
Лапароскопический метод операции считается более щадящим для организма и постоперационный период реабилитации значительно короче. Кроме того, людям которые имеют противопоказания к открытому хирургическому вмешательству или уже перенесли операцию грыжесечения, рекомендуется лапароскопия.
Подготовка к операции включает сдачу необходимых анализов, консультацию у специалистов и диагностику выпячивания. За восемь часов до операции нельзя употреблять пищу и пить много жидкости, больному делается клизма.
Во время операции, больному делается небольшой надрез в паховой области и вводится специальный прибор — лапароскоп. Прибор присоединен к камере, которая на мониторе позволяет врачу контролировать ход операции. Для осмотра содержимого грыжевого мешка в нем делаются проколы и проводится диагностика состояния внутренних органов. После всех манипуляций больному накладывают шов. Операция проводится под общим наркозом и требует высокой квалификации лечащего врача.
Операция имеет ряд противопоказаний:
- нарушение свертываемости крови;
- сердечно-сосудистые заболевания;
- воспалительные процессы тканей в области возникновения грыжи.
Диагностика и лечение паховой грыжи у женщин проходит также, как и у мужчин. Исключение составляет возникновение грыжи при беременности. Во время вынашивания ребенка операция грыжесечения не проводится. Для предотвращения осложнений и роста выпячивания, женщина должна носить бандаж и ограничить любые физические нагрузки.
Паховая грыжа не несет опасность роженице и ее ребенку и никак не влияет на внутриутробное развитие плода. Кроме того, выполняя врачебные предписания во время беременности, роды проходят естественным путем. В редких случаях, когда грыжа постоянно увеличивается в размерах и во время потуг может произойти ущемление, пациентке делают кесарево сечение.
источник
Изобретение относится к медицине, а именно к хирургии, и может быть использовано при лапароскопической паховой герниопластике у больных с прямой паховой грыжей.
Наиболее часто встречающимися осложнениями лапароскопической паховой герниопластики является псевдорецидив и серома. Эти осложнения связаны с тем, что перерастянутая поперечная фасция в области пахового промежутка пролабирует через наружное отверстие пахового канала после операции и вызывает опухолевидную деформацию, напоминающую рецидив грыжи. При скоплении тканевой жидкости между сетчатым эндопротезом и поперечной фасцией образуется серома, которая увеличивает сроки реабилитации, часто требует пункционного лечения, симулирует рецидив заболевания.
Наиболее распространенным способом профилактики описанных осложнений при лапароскопической паховой герниопластике является фиксация поперечной фасции в виде тяжа к связке Купера (Егиев В.Н., Воскресенский П.К. Грыжи. – М.: Медпрактика-М., 2015. – 480 с.). Способ осуществляется следующим образом. Делают Г-образный разрез брюшины паховой области, мобилизуют нижний лоскут брюшины, выделяют грыжевой мешок. Инструментом захватывают поперечную фасцию и фиксируют герниостеплером к связке Купера одной или двумя клипсами. Далее укладывают сетчатый эндопротез, закрывая все слабые места паховой области, фиксируют его и ушивают над ним брюшину. Способ прост в исполнении, но имеет недостатки. Для фиксации поперечной фасции используется дополнительные одну-две клипсы-спирали, что увеличивает количество металла в организме, а также способствует формированию хронического болевого синдрома у некоторых больных. Сетчатый эндопротез при описанном способе не прилегает к связке Купера на всем протяжении. Между ними имеет место интерпозиция поперечной фасции, что увеличивает вероятность рецидива.
Известен способ укрепления пахового канала при прямой паховой грыже путем пластики поперечной фасции эндопетлей (RU 2498778 C2, 20.11.2013.). Способ осуществляется следующим образом. Делают Г-образный разрез брюшины паховой области, мобилизуют нижний лоскут брюшины, выделяют грыжевой мешок. Инструментом захватывают поперечную фасцию и путем скручивания образуют тяж из неё, который лигируют эндопетлей у основания. Основным недостатком способа является то, что образуется достаточно большая масса тканей дистальнее эндопетли, которая подвергается некрозу в послеоперационном периоде, так как лишена кровоснабжения. Кроме того, в петлю при таком способе могут попасть элементы семенного канатика, которые расположены непосредственно на ней, а это может привести к некрозу яичка и развитию бесплодия у пациентов мужского пола.
Техническим результатом изобретения является профилактика серомы при эндовидеохирургическом лечении прямой паховой грыжи.
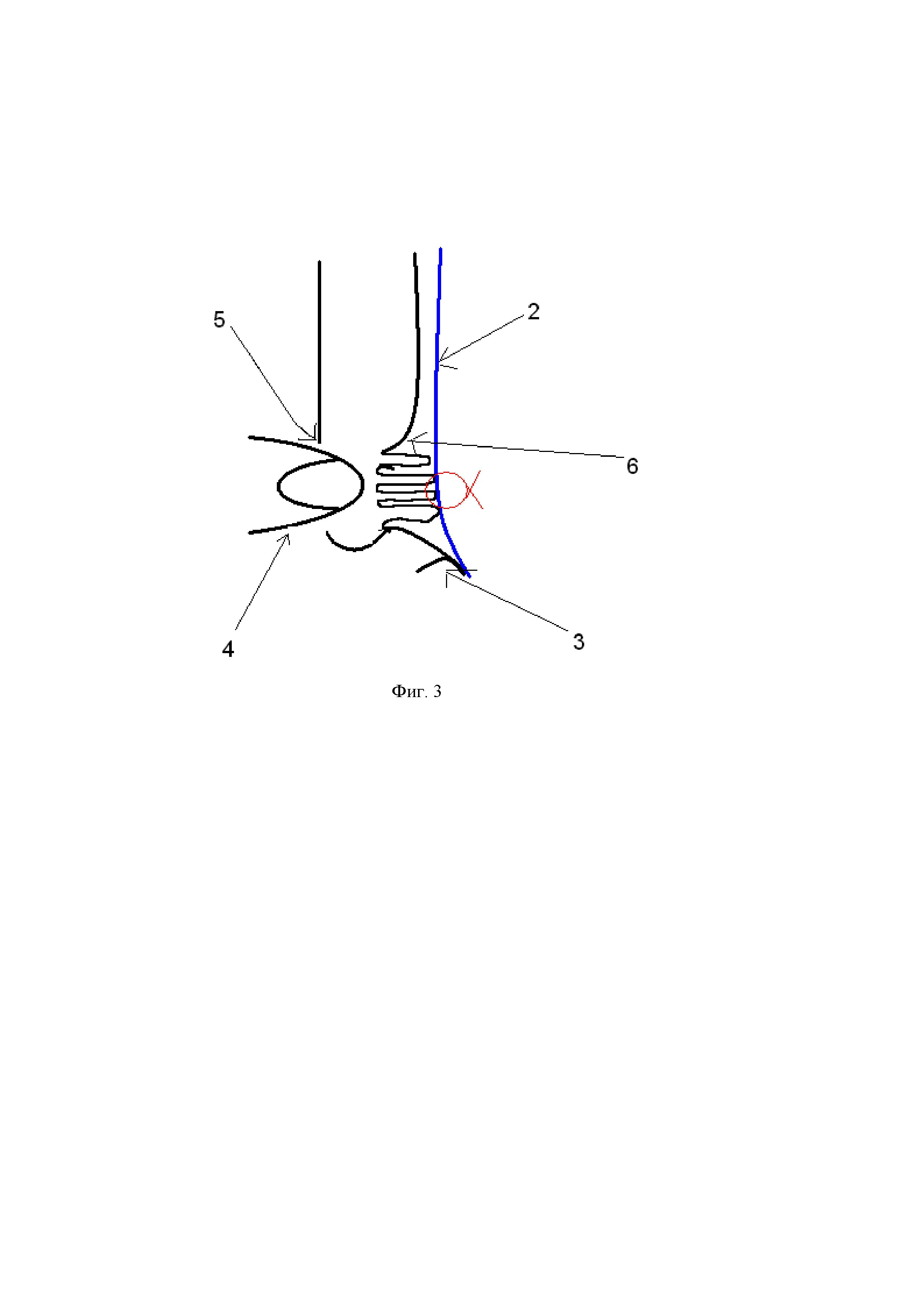
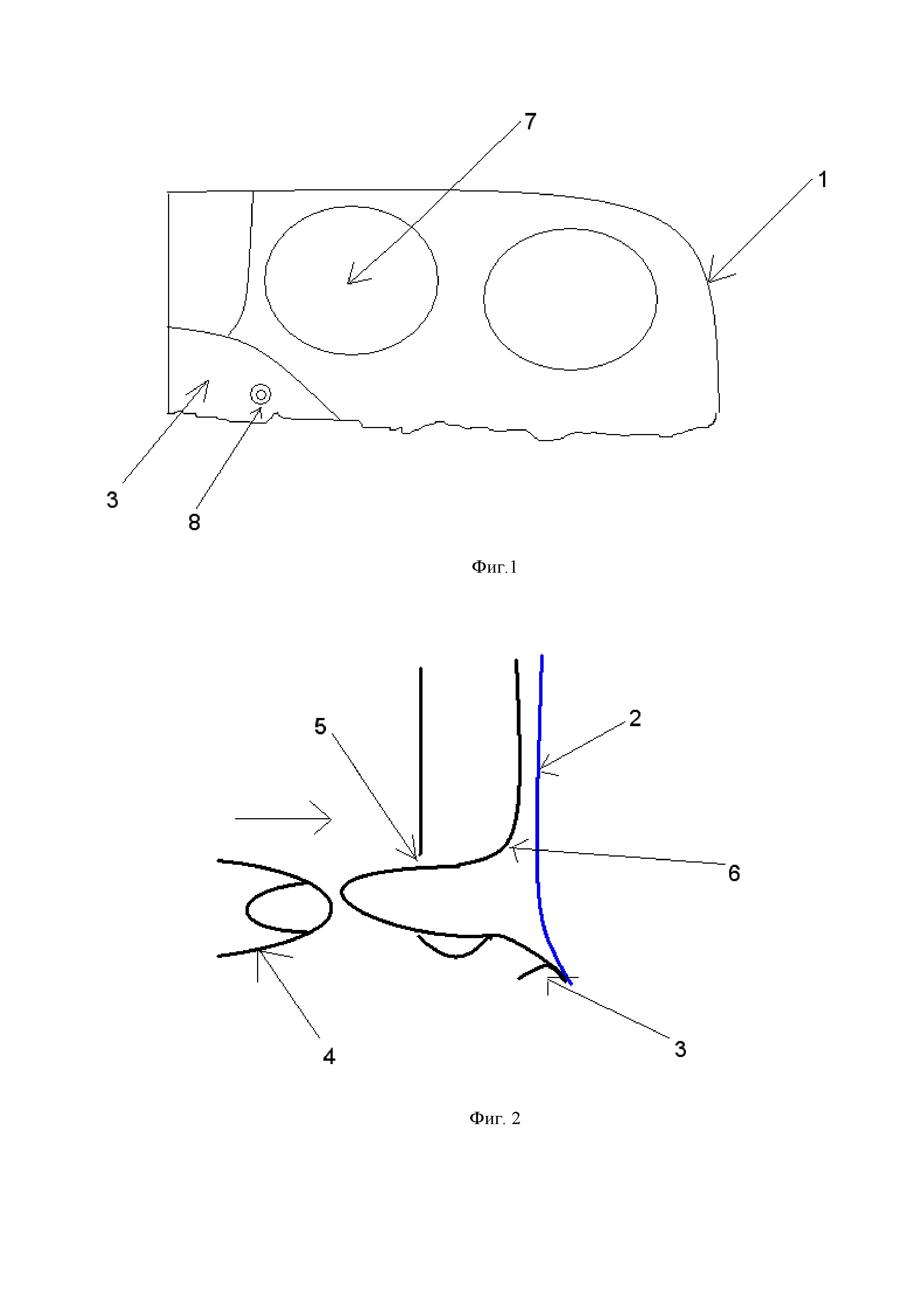
Способ заключается в следующем. Делают Г-образный разрез (1) брюшины паховой области, мобилизуют нижний лоскут брюшины, выделяют грыжевой мешок. В паховой области укладывают сетчатый эндопротез (2), который закрывает все слабые места в данной зоне, фиксируют к связке Купера (3) спиральной клипсой (8). Осуществляют мануальное вправление (4) поперечной фасции (6) в наружное отверстие пахового канала (5) таким образом, чтобы перерастянутая поперечная фасция (6) соприкасалась с сетчатым эндопротезом (2) в области медиальной паховой ямки (7). Далее накладывают один или два поверхностных шва (8), в зависимости от размера грыжевого мешка на поперечную фасцию в центре медиальной паховой ямки (7) непосредственно через эндопротез (2), не прекращая давление пальцем со стороны кожи, вяжут интракорпоральный узел.
Способ апробирован на 11 пациентах трудоспособного возраста 32-41 год. Длительные наблюдения в отдаленном послеоперационном периоде позволили выявить следующие неочевидные эффекты предложенного способа: ранний восстановительный период согласно классическим канонам герниопластики составляет не менее 14 дней, при использовании предложенного способа он составил не более 10 дней; избегание половой жизни в группе контроля не менее 20 дней, в группе исследования не более 11-12 дней.
При таком способе имеют место перечисленные ниже эффекты.
Ликвидируется остаточная полость между сетчатым эндопротезом и поперечной фасцией, что препятствует образованию серомы в этой области.
Увеличивается надежность фиксации сетчатого эндопротеза за счет его сшивания с поперечной фасцией.
Пример 1. Больной В., 76 лет. Поступил в плановом порядке с жалобами на опухолевидное образование в правой паховой области. На лапароскопической операции диагностирована прямая паховая грыжа. Выполнено выделение брюшины, грыжевого мешка. Поперечная фасция растянута. Полипропиленовый сетчатый эндопротез размерами 10х15 см расположен в паховой области и фиксирован к связке Купера. Поперечная фасция в центре медиальной паховой ямки фиксирована к протезу указанным способом. Дополнительной фиксации эндопротеза не потребовалось. Брюшина ушита интракорпоральным швом. Течение послеоперационного периода без особенностей. Контрольное ультразвуковое исследование на 3-и сутки после операции пред выпиской из стационара. Данных за наличие серомы нет. Больной осмотрен через 12 месяцев. Рецидива грыжи не отмечено, жалоб нет.
Пример 2. Больной К., 25 лет. Поступил в плановом порядке с жалобами на опухолевидные образования в паховых областях. На операции диагностирована двусторонняя прямая паховая грыжа. Выполнено выделение брюшины, грыжевых мешков с двух сторон. Поперечная фасция растянута. Полипропиленовые сетчатые эндопротезы размерами 10х15см каждый расположены в паховых областях и фиксированы к связкам Купера. Поперечная фасция в центре медиальной паховой ямки с двух сторон фиксирована к протезу указанным способом. Дополнительной фиксации эндопротезов не потребовалось. Брюшина ушита интракорпоральным швом. Течение послеоперационного периода без особенностей. Контрольное ультразвуковое исследование на 3-и сутки после операции пред выпиской из стационара. Данных за наличие сером с двух сторон нет. Больной осмотрен через 12 месяцев. Рецидива грыжи не отмечено, жалоб нет.
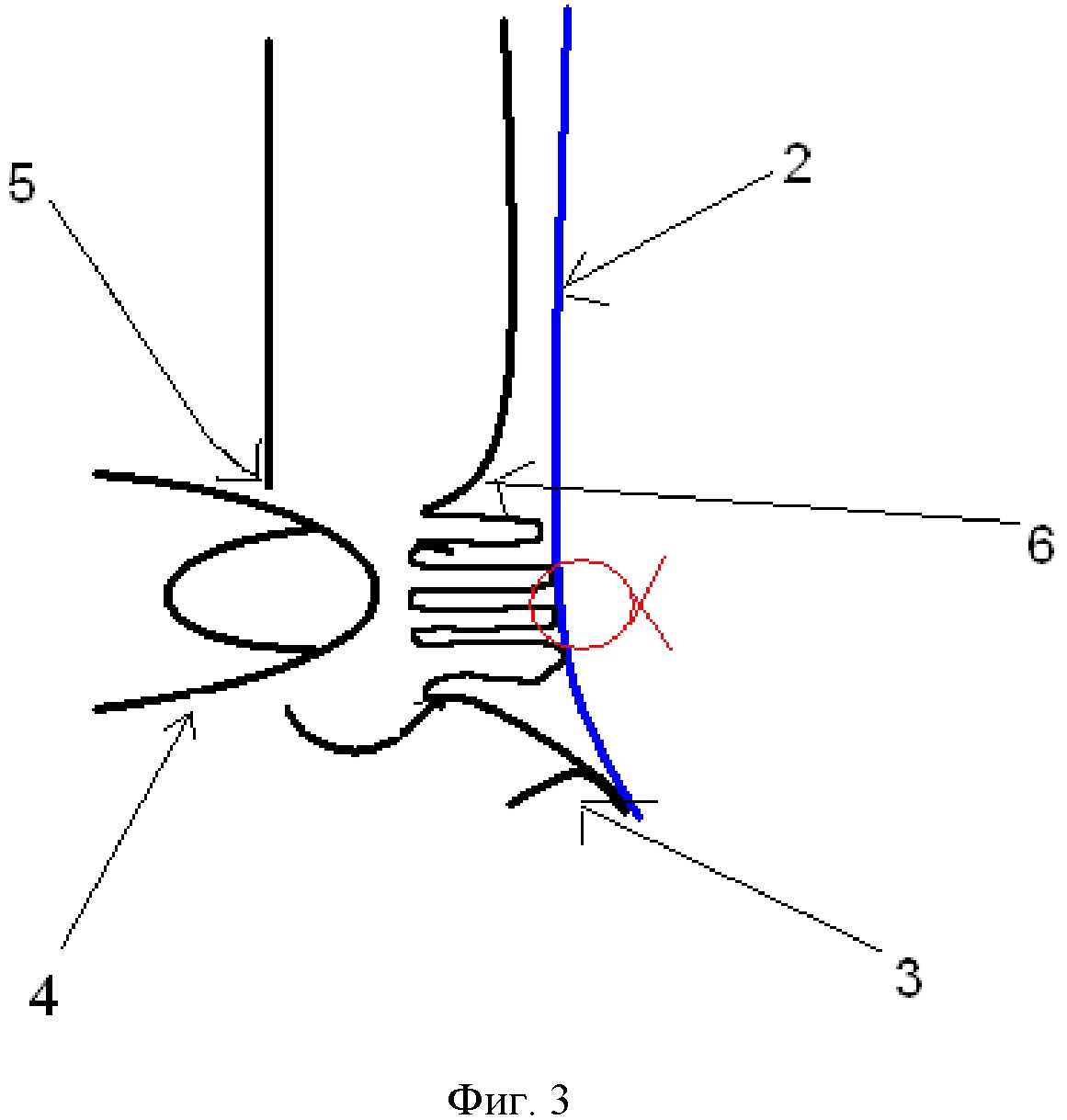
Фигура 1. Схема правой паховой области со стороны брюшной полости.
1 – Г-образный разрез брюшины
7 – медиальная паховая ямка
Фигура 2. Схема сагиттального среза паховой области .
5 – наружное отверстие пахового канала
Фигура 3. Схема сагиттального среза паховой области после наложения шва.
5 – наружное отверстие пахового канала
Способ профилактики серомы при лапароскопической паховой герниопластике прямой паховой грыжи, при котором выполняют рассечение брюшины, мобилизуют нижний ее лоскут, выделяют грыжевой мешок, укладывают сетчатый эндопротез в паховой области, фиксируют его к связке Купера у медиального края спиральной клипсой, отличающийся тем, что осуществляют мануальное вправление поперечной фасции в наружное отверстие пахового канала до соприкосновения с сетчатым эндопротезом, фиксируют поперечную фасцию к эндопротезу в центре медиальной паховой ямки узловым интракорпоральным швом, ушивают разрез брюшины.
Способ оценки натяжения в апоневротическом слое лапаротомной раны и устройство для его осуществления
Изобретение относится к медицине и может быть использовано как интраоперационно, так и на кадаверином материале для оценки тензометрических свойств передней брюшной стенки. На края апоневротической раны накладывают пластины определенного размера с шипами и сводят пластины друг по направлению к.
источник
Многие годы пытаетесь вылечить СУСТАВЫ?
Глава Института лечения суставов: «Вы будете поражены, насколько просто можно вылечить суставы принимая каждый день.
Межпозвонковая грыжа относится к часто встречающимся патологиям опорно-двигательной системы. В отсутствие лечения это заболевание может привести к инвалидизации пациента. Современная медицина предлагает различные варианты лечения межпозвонковой грыжи.
Для лечения суставов наши читатели успешно используют Артрейд. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
В русскоязычном интернете более распространен термин «межпозвоночная грыжа». Это название патологии не совсем корректно с точки зрения медицины, но оно настолько прижилось, что нередко даже невропатологи начинают употреблять такой термин в общении с пациентами.
Межпозвонковая грыжа – это выпячивание диска. В норме он представляет собой амортизирующую прослойку между позвонками и обеспечивает подвижность позвоночного столба.
Когда физические нагрузки на позвоночник становятся чрезмерными, или дебютируют дегенеративные процессы в этой области, диск начинает выпячиваться. Как правило, со временем он возвращается на место. Эта патология носит название протрузии. Она также сопровождается неврологическими симптомами, но случается это реже.
В отсутствие лечения происходит разрыв фиброзного кольца, и образуется стойкий пролапс диска. Это и называется межпозвонковой грыжей.
Постоянное выпячивание диска со временем все сильнее сдавливает окружающие структуры и у пациента возникают разнообразные неврологические симптомы.
Не все грыжи одинаково опасны. Наиболее неблагоприятный прогноз у тех выпячиваний, что направлены в сторону спинного мозга и грозят его сдавлением. Возникновение боковых межпозвонковых грыж чревато ущемлением нервных корешков – различными радикулопатиями.
Выбор метода лечения межпозвонковых грыж зависит от следующих факторов:
- Локализации и направленности выпячивания.
- Степени выраженности неврологических симптомов.
- Эффективности предшествующей терапии.
- Длительности временной нетрудоспособности пациентов в течение прошедших 1–2 лет.
Как правило, невропатологи предпочитают консервативные методы лечения этой патологии. Они включают в себя:
- Использование медикаментозных препаратов (НПВС, миорелаксантов, антиконвульсантов в случае присоединения нейропатической боли).
- Лечебную физкультуру и кинезитерапию. Упражнений должно быть много и на регулярной основе.
- Физиотерапевтические методы (магнитотерапию, дарсонваль, УВЧ, электрофорез и другие).
При отсутствии эффекта от консервативной терапии, пациент направляется на консультацию нейрохирурга для решения вопроса о целесообразности оперативного вмешательства.
В отличие от консервативной терапии, хирургическое вмешательство показано далеко не во всех случаях.
Так, при межпозвонковых грыжах шейного отдела операция рекомендуется крайне редко в связи с высоким риском различных осложнений после удаления выпячивания. При грыжах поясничного отдела, наоборот, хирургическое вмешательство оказывает выраженный и стойкий лечебный эффект.
Часто пациентов интересует период восстановления после операции – пребывание в стационаре и количество дней больничного листа после выписки. Это зависит от стадии патологического процесса, доступа и объема оперативного вмешательства.
В течение длительного времени основными методами оперативного лечения межпозвонковой грыжи являлись:
Первые два варианта операций выполняются при помощи переднего доступа, а дискэктомия – заднего, бокового или переднего в зависимости от расположения образования. С этим связаны и различные сроки пребывания на больничном листе после хирургического лечения.
Оперативное вмешательство при помощи заднего доступа позволяет провести интерламинэктомию и гемиламинэктомию, а также фенестрацию.
Целью такого хирургического лечения является декомпрессия диска, которая бывает открытой и закрытой. Как только дегенеративно измененный диск прекращает сдавливать близлежащие структуры – нервные корешки или спинной мозг, у пациента быстро наступает улучшение самочувствия. Исчезают хронические боли в области спины, двигательные и чувствительные расстройства.
На сколько дают больничный после операции при грыже позвоночника? В среднем, сроки временной нетрудоспособности при таких вмешательствах колеблются от одного до двух месяцев. Точнее сказать, сколько дней продлится больничный лист у конкретного пациента, можно только после хирургического лечения.
Ламинэктомия и ее варианты – это удаление фрагмента позвонка и части межпозвонкового диска над сдавливаемым нервным корешком. Таким образом, устраняется ущемление и симптомы радикулопатии.
Ламинэктомию еще называют открытой декомпрессией. Иногда одновременно проводится и резекция желтой связки. Это достаточно травматичный метод лечения. Он требует нахождения в стационаре в течение 5–7 дней, а также временной иммобилизации позвоночника.
Больничный лист после ламинэктомии врачи предпочитают давать длительный, на 1–2 месяца. В случае если неврологическая симптоматика сохраняется, больничный может быть продлен до 3–4 месяцев, после чего пациенту дают направление на медико-социальную экспертизу для утверждения стойкой нетрудоспособности.
Даже после выхода на работу, первые 2–3 месяца пациенту рекомендовано носить полужесткий корсет.
В настоящее время ламинэктомия при межпозвонковых грыжах применяется очень редко, обычно в том случае, если они расположены на уровне поясницы. Чаще этот метод используют при спинальном стенозе.
Фенестрация относится к более щадящим методам оперативного вмешательства. Она включает в себя хирургическое иссечение и удаление измененных частей диска, его пульпозного ядра.
Такое лечение намного легче переносится пациентом, ходьба разрешается врачом уже в течение первых суток после операции. Как правило, в длительном нахождении в стационаре нет необходимости. Прооперированный человек может вернуться домой спустя 1–3 дня.
Сколько длится больничный после фенестрации? В течение 4–8 недель не рекомендованы наклоны, длительное пребывание в сидячем положении, тяжелые нагрузки. Иногда требуется временная иммобилизация позвоночника, которая обеспечивается ношением жесткого корсета.
Больничный лист врач может дать на весь этот период, если работа пациента предполагает физическую активность. При хорошем самочувствии, отсутствии болей и неврологической симптоматики срок временной нетрудоспособности может быть сокращен до 3–4 недель.
Ранее больничный лист после дискэктомии был достаточно длительным. Эта операция проводилась при помощи переднего доступа и была обширной.
Дискэктомия, или удаление диска, обычно дополнялась передним спондилодезом. Это хирургическое вмешательство, при котором между смежными позвонками создается неподвижность за счет установки костного трансплантата. Насколько оно травматично?
При дискэктомии с передним спондилодезом лечение в больнице может занимать от 1,5 до 2 месяцев. Длительный больничный связан с необходимостью формирования костного анкилоза – консолидации. После выписки из стационара пациент переходит под амбулаторное наблюдение невропатолога или нейрохирурга, и его нетрудоспособность может продолжаться от 6 до 8 месяцев. Решение о продлении больничного листка принимает лечащий врач совместно с врачебно-консультативной комиссией.
При необходимости пациент направляется на МСЭК, где требуется пройти освидетельствование, и по данным результатам получить на 1 год инвалидность.
Однако за последние годы в нейрохирургии отметился существенный прогресс. Современные операции менее травматичны и не требуют длительного нахождения на больничном листе. К ним относятся:
В отличие от обычной операции, микродискэктомия представляет собой микрохирургическое удаление диска. Выполняется она под контролем микроскопа.
Целью микродискэктомии является декомпрессия спинного мозга либо нервного корешка. За счет этого ликвидируются неврологические симптомы, восстанавливается чувствительность, уменьшаются болевые ощущения.
Разрез при микродискэктомии небольшой, окружающие ткани страдают мало. Этим объясняется и короткий восстановительный период после операции – не более 3–5 дней. Дальнейшее наблюдение в условиях больницы не требуется, и пациент находится на амбулаторном больничном листке. В среднем это продолжается 15–20 дней.
Также существует эндоскопическая микродискэктомия.
Эта операция по праву считается золотым стандартом хирургического лечения межпозвонковых грыж. Проводится она с использованием эндоскопа, благодаря чему нет необходимости в разрезах кожи и мягких тканей. Для введения хирургического инструмента достаточно обычных проколов, поскольку его диаметр не превышает 7 мм.
Неврологическая симптоматика после проведения эндоскопической микродискэктомии исчезает уже в течение суток, и это время пациенту совсем необязательно проводить лежа в постели. Сразу после операции ему разрешена и показана легкая физическая активность.
Госпитализация, как правило, длится не более 1–2 дней. Амбулаторный лист нетрудоспособности составляет 10–20 дней – в зависимости от состояния здоровья пациента.
Эта процедура представляет собой воздействие лазера на дегенеративно измененный диск, вследствие чего он частично разрушается. Размеры выпячивания уменьшаются и, таким образом, достигается декомпрессия диска.
Для лечения суставов наши читатели успешно используют Артрейд. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Лазерная вапоризация относится к малоинвазивным методам лечения межпозвонковых грыж, однако она эффективна лишь на ранних стадиях заболевания. На следующий день пациент выписывается из больницы и переходит под наблюдение невропатолога, который выдает ему больничный лист на 2–3 недели.
Протезирование межпозвонкового диска относится к современным и высокоэффективным операциям. При этом происходит полная замена дегенеративно измененных структур на эндопротез.
Новый диск выполняет все те функции, что и удаленный. Благодаря этой операции сохраняется мобильность позвоночного столба. Кроме того, оперативное вмешательство эффективно устраняет болевой синдром и неврологическую симптоматику, а также разгружает соседние позвонки.
Часто диск заменяют не полностью, а лишь его пульпозное ядро. Для этой цели используют специальные синтетические вкладки.
Восстановление после эндопротезирования достаточно быстрое. Пребывание в больнице длится не больше пяти дней, если удалялась межпозвонковая грыжа в поясничном отделе, и двух-трех дней при ее расположении на уровне шеи. Амбулаторный больничный лист длится в среднем 2–3 недели.
источник
Общие принципы лечения пациентов после пластики грыжевых ворот местными тканями практически не имеют отличий ведения послеоперационного периода при других заболеваниях. Для профилактики дыхательных осложнений, послеоперационного пареза кишечника и тромбоэмболических осложнений проводят раннюю активизацию пациента. Кроме того, для профилактики тромбоэмболии лёгочной артерии показано применение компрессионного госпитального трикотажа и введение антикоагулянтов до полной активизации пациента. Антибактериальную профилактику с однократным внутривенным введением антибиотика за 1 ч до операции проводят пациентам с высоким риском инфекционных осложнений. Основными показаниями к введению антибиотиков в послеоперационном периоде служат наличие воспалительного инфильтрата или гематомы операционной раны, гипертермия, а также лечение воспалительных осложнений со стороны других органов и систем.
При применении синтетических эксплантатов, особенно при их расположении над апоневрозом, течение послеоперационного периода имеет свои особенности. Эти отличия — следствие широкой мобилизации кожных лоскутов и подкожной клетчатки от передней поверхности влагалищ прямых мышц или апоневроза наружной косой мышцы живота и наличия инородного тела в ране. Возникающие при этом нарушения оттока венозной крови и лимфы из подкожной клетчатки приводят к скоплению в ране большого количества серозного отделяемого и замедлению её заживления.
С целью профилактики образования сером необходимо проводить активное дренирование раневой полости двумя дренажами, расположенными между подкожной жировой клетчаткой и эксплантатом, сроком на 1-2 сут. Одновременно с активным дренированием используют дозированную компрессию раны при помощи эластичного бандажа, который позволяет равномерно прижимать кожные лоскуты к поверхности эксплантата, а брюшной стенке — полноценно участвовать в процессе дыхания. В последующем происходит постепенное уменьшение количества раневого отделяемого и его организация. Дополнительное удаление раневого отделяемого необходимо проводить при помощи пункций с частотой 1-2 раза в течение 10 дней.
Ношение эластичного бандажа после выполнения пластики передней брюшной стенки с применением синтетических эксплантатов показано в течение 1-2 мес. Использование бандажа в большие сроки нецелесообразно из-за ослабления мышц передней брюшной стенки и показано только при выполнении пациентом физической нагрузки. Приступать к физическому труду пациентам рекомендуется не ранее чем через 2-3 мес после выполнения оперативного вмешательства.
Причины возникновения послеоперационных осложнений достаточно многообразны и могут быть обусловлены как неправильным выбором метода пластики грыжевых ворот, так и нарушениями техники выполнения оперативного вмешательства. Все осложнения после выполнения грыжесечений условно разделяют на две большие группы: осложнения ближайшего и отдалённого послеоперационного периода.
Наиболее типичные осложнения раннего послеоперационного периода — местные раневые осложнения: гематома, воспалительный инфильтрат и нагноение. Серома послеоперационной раны после проведения оперативных вмешательств с использованием синтетических эксплантатов не расценивается в качестве раневого осложнения; серома — следствие закономерной реакции жировой клетчатки на имплантацию синтетического инородного материала. При этом необходимо отметить, что пластика пахового канала по сравнению с пластикой передней брюшной стенки при вентральных грыжах сопровождается значительно меньшей частотой возникновения сером. Это связано как с более низкой агрессивностью хирургического вмешательства, так и с расположением эксплантата под апоневрозом без контакта его с жировой клетчаткой. Кроме того, минимальную частоту возникновения сером отмечают при применении методики эксплантации «sublay» и применении эксплантатов из полипропилена.
Гематома послеоперационной раны — следствие неадекватного гемостаза. Необходимо отметить, что при пластике передней брюшной стенки с применением эксплантатов требования к качеству выполнения гемостаза значительно возрастают. Это связано с тем, что применение данного вида пластики не позволяет надеяться на сдавление и тампонирование кровоточащих сосудов и может сопровождаться формированием обширных гематом. Основными мероприятиями, направленными на профилактику образования гематом, служат тщательный гемостаз, минимизация травматизации тканей передней брюшной стенки при их подготовке к эксплантации, применение в первые сутки после оперативного вмешательства компрессионных повязок и местной гипотермии.
Особое место в структуре послеоперационных осложнений после выполнения пластики с применением синтетических эксплантатов занимают гнойно-септические осложнения; они определяют особые требования к ведению пациентов. При появлении признаков нагноения послеоперационной раны производят разведение её краёв с применением тактики лечения в соответствии с классическими канонами гнойной хирургии. В случаях применения эксплантатов, изготовленных из монофиламентной нити, их удаляют только при формировании неподдающихся лечению гнойных свищей. При этом далеко не всегда иссекают весь эксплантат, чаще ограничиваются его резекцией.
Большое значение для профилактики развития раневых гнойно-септических осложнений имеет соблюдение принципов асептики. Недопустимо применение эксплантатов, стерилизация которых проводилась не в заводских условиях, и тем более после повторной стерилизации. Кроме того, фиксацию эксплантата и ушивание операционной раны также необходимо проводить инертным шовным материалом, прошедшим качественную заводскую обработку.
Нагноение послеоперационной раны может быть обусловлено и нарушениями техники выполнения хирургического вмешательства: отсутствием герметичности послеоперационной раны и мест установки дренажей, несоблюдением принципов постоянной аспирации раневого отделяемого. В этих случаях необходимо применение глухого шва послеоперационной раны, тщательный контроль за эффективностью функционирования дренажей и их раннее удаление (на 2-е-З-и сутки после выполнения оперативного вмешательства) с последующим выполнением пункций остаточной полости.
При проведении пластики с натяжением тканей и перемещении содержимого грыжевого мешка в брюшную полость, в особенности при уменьшении её объёма, развивается повышение внутрибрюшного давления, которое определяет ряд системных нарушений (табл. 68-3).
Таблица 68-3. Функциональные нарушения при абдоминальном компартмент-синдроме
| Система | Функциональные нарушения |
| Сердечно-сосудистая | Снижение венозного возврата крови, увеличение общего периферического сосудистого сопротивления, снижение сердечного выброса, увеличение ЦВД и давления заклинивания лёгочной артерии |
| Система дыхания | Увеличение пикового инспираторного давления, увеличение сопротивления, гипоксемия, гиперкапния, ацидоз, снижение динамического комплаенса |
| Система мочеотделения | Снижение почечного кровотока, снижение клубочковой фильтрации, снижение реабсорбции глюкозы, олигурия или анурия |
| Система пищеварения | Снижение перфузионного давления органов желудочно-кишечного тракта, снижение мезентериального кровотока, парез кишечника |
| Центральная нервная система | Повышение внутричерепного давления, снижение перфузионного давления головного мозга |
Наиболее грозное осложнение резкого повышения давления в брюшной полости после выполнения пластики передней брюшной стенки — абдоминальный компартмент-синдром, характеризующийся развитием полиорганной недостаточности.
В зависимости от уровня повышения внутрибрюшного давления выделяют четыре степени абдоминального компартмент-синдрома:
- I степень — 10-15 мм рт.ст.;
- II степень — 15-25 мм рт.ст.;
- III степень — 25-35 мм рт.ст.;
- IV степень — более 35 мм рт.ст.
У пациентов после выполнения плановых лапаротомий давление в брюшной полости может достигать I степени без развития клинических признаков абдоминального компартмент-синдрома, а при повышении внутрибрюшного давления до 35 мм рт.ст. и выше он развивается в 100% клинических наблюдений с высоким риском летального исхода. Критериями абдоминального компартмент-синдрома считают увеличение внутрибрюшного давления свыше 15 мм рт.ст. и ацидоз в сочетании с такими признаками (одним или более), как гипоксемия, повышение ЦВД или давления заклинивания лёгочных артерий, снижение АД или сердечного выброса, олигурия.
Клинические симптомы проявления абдоминального компартмент-синдрома неспецифичны. Ежедневный осмотр и пальпация живота также не дают точных представлений о величине внутрибрюшного давления. В связи с этим для специфической диагностики абдоминального компартмент-синдрома в раннем послеоперационном периоде необходимо проводить ежедневный мониторинг внутрибрюшного давления, которое может быть измерено как прямым методом посредством дренажей, так и непрямыми методами через полость желудка, в бедренной вене или в мочевом пузыре.
Наиболее простой способ определения давления в брюшной полости — измерение давления внутри мочевого пузыря. Хорошо растяжимая и эластичная стенка мочевого пузыря при объёме содержимого не более 100 мл выполняет функцию пассивной мембраны и с высокой точностью отражает внутрибрюшное давление. Техника измерения внутрибрюшного давления аналогична таковой при определении ЦВД. При измерении давления пациент должен находиться в положении лёжа на спине строго на горизонтальной поверхности. Для определения давления используют мочевой катетер Фолея, через который в мочевой пузырь вводят 50-100 мл стерильного 0,9% раствора натрия хлорида. Величину давления оценивают по уровню жидкости в сообщающемся капилляре при помощи измерительной линейки, принимая за ноль верхний край лонного сочленения. При угрозе развития данного синдрома внутрибрюшное давление необходимо измерять каждые 2-4 ч, не дожидаясь появления его первых клинических признаков.
Избежать развития абдоминального компартмент-синдрома позволяет, главным образом, правильный выбор адекватного способа пластики грыжевых ворот. Определённую роль отводят также профилактике развития пареза кишечника. Единственный эффективный метод лечения уже развившегося абдоминального компартмент-синдрома — хирургическая декомпрессия, достоверно снижающая летальность; её необходимо выполнять по жизненным показаниям даже после пластики передней брюшной стенки. Без проведения хирургической декомпрессии летальность больных с IV степенью абдоминального компартмент-синдрома достигает 100%.
Рецидив грыжи — одно из поздних осложнений операции грыжесечения. Основные причины возврата заболевания — слабость собственных тканей пациента, технические погрешности выполнения операции, а также чрезмерные физические нагрузки при отсутствии сформированного прочного рубца.
Чрезмерное натяжение сшиваемых тканей — основная причина рецидива грыжи. Неоспоримым считают факт, что частота рецидива значительно ниже при ненатяжной пластике с использованием синтетических эксплантатов. Рецидив грыжи при пластике эксплантатом развивается в результате смещения сетки или выхождения грыжевого образования через не укреплённый сеткой дефект апоневроза. Смещение сетки обычно происходит из-за её частичного или полного отрыва в результате нарушения техники её фиксации или в результате резкого повышения внутрибрюшного давления в ранние сроки после операции, когда ещё не образовался достаточно прочный рубец, удерживающий сетку.
Основными нарушениями техники фиксации эксплантата служат:
- использование нитей малых диаметров или только герниостеплеров, что приводит к отрыву эксплантата при кашле или физической нагрузке;
- фиксация эксплантата к изменённым тканям;
- выраженное натяжение тканей с последующим их «прорезыванием»;
- недостаточная площадь соприкосновения эксплантата и собственных тканей пациента.
К поздним осложнениям после выполнения пластики относят инфильтраты и свищи послеоперационной раны, которые возникли после выписки пациента из стационара при неосложнённом течении раннего послеоперационного периода. В этих случаях при безуспешности консервативной терапии удаляют или резецируют эксплантат и дренируют рану.
Невралгия после выполнения стандартных видов пластики — достаточно редкое осложнение. Её развитие, как правило, связано с погрешностями хирургической техники выполнения пластики и, в частности, с попаданием в шов нервных стволов или их сдавлением. Для предупреждения возникновения невралгий во время выполнения хирургического вмешательства необходима отчётливая визуализация нервных стволов, а фиксацию эксплантата необходимо выполнять швами, параллельными ходу нервных стволов. Кроме того, прорастание эксплантата соединительной тканью и образование плотной рубцовой ткани с вовлечением в процесс нервных волокон также считают одной из причин возникновения болевого синдрома в позднем послеоперационном периоде.
При возникновении хронической невралгии проводят консервативную терапию, включающую введение нестероидных противовоспалительных препаратов, витаминов группы В и физиотерапевтическое лечение. При неэффективности консервативной терапии выполняют повторное хирургическое вмешательство, направленное на полное или частичное удаление эксплантата или невротомию.
В истории развития учения об оперативном лечении наружных брюшных грыж примечателен кардинальный перелом, наступивший на рубеже прошлого и нынешнего столетий. Конструктивная критика отдельных традиционно утвердившихся оперативных приёмов привела к их переоценке и пересмотру основ современной герниологии. Кроме того, оперативная техника обогатилась эндоскопическими технологиями и принципиально новыми методами аллопластики с применением надёжных биологически инертных синтетических материалов. Удалось значительно расширить возможности радикального излечения вентральных, послеоперационных и рецидивных грыж с чрезмерным дефектом мышечных и апоневротических тканей, которые считались не поддающимися лечению. Современные технологии лечения стали доступными широкому кругу хирургов. Такая демократизация оперативного метода здесь особенно важна, поскольку речь идёт о лечении болезни, занимающей видное место в повседневной хирургической практике.
источник
Ведение пациентов с серомами после грыжесечений в раннем послеоперационном периоде Текст научной статьи по специальности « Медицина и здравоохранение»
Аннотация научной статьи по медицине и здравоохранению, автор научной работы — Кузнецов Алексей Владимирович, Шестаков Вячеслав Васильевич, Алексеев Борис Викторович
Целью исследования явилось изучение ближайших результатов лечения больных с послеоперационными вентральными грыжами, послеоперационный период которых протекал с серомами подкожной клетчатки, при различных способах их санации. Оптимальным для лечения сером после аллопластики инцизионных грыж является пункционный способ. Это проявляется в более скором исчезновении экстравазата, минимальном риске инфицирования полости серомы и более благоприятном и краткосрочном восстановительном периоде.
Похожие темы научных работ по медицине и здравоохранению , автор научной работы — Кузнецов Алексей Владимирович, Шестаков Вячеслав Васильевич, Алексеев Борис Викторович,
The aim. of the research was to study the nearest results of treatment of patients with postoperative ventral hernias which had. postoperative period with seromas of subcutaneous cellular tissue at different ways of their sanation. Optimal way for treatment of seromas after the alloplasty of incisional hernias is puncture. It shows up in quicker disappearance of extravasate, minimal risk of contamination of seroma cavity and more favorable and short-term restorative period.
Текст научной работы на тему «Ведение пациентов с серомами после грыжесечений в раннем послеоперационном периоде»
А.В. Кузнецов 2, В.В. Шестаков Б.В. Алексеев 1
ВЕДЕНИЕ ПАЦИЕНТОВ С СЕРОМАМИ ПОСЛЕ ГРЫЖЕСЕЧЕНИЙ В РАННЕМ ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ
1 Новосибирский государственный медицинский университет (Новосибирск) 2 Городская клиническая больница № 2 (Новосибирск)
Целью исследования явилось изучение ближайших результатов лечения больных с послеоперационными вентральными, грыжами, послеоперационный период которых протекал с серомами подкожной клетчатки, при различных способах их санации.
Оптимальным для лечения, сером, после аллопластики, инцизионных грыж является, пункционный способ. Это проявляется, в более скором, исчезновении, экстравазата, минимальном, риске инфицирования полости серомы и более благоприятном и краткосрочном, восстановительном периоде.
Ключевые слова: серома, полипропиленовый сетчатый протез, ранний послеоперационный период
TREATMENT OF PATIENTS WITH SEROMAS AFTER HERNIOTOMIES IN EARLY POSTOPERATIVE PERIOD
A.V. Kuznetsov 1- 2, V.V. Shestakov 1, B.V. Alekseev 1 2
1 Novosibirsk State Medical University, Novosibirsk
2 Municipal Clinical Hospital N 2, Novosibirsk
The aim. of the research was to study the nearest results of treatment of patients with postoperative ventral hernias which had. postoperative period, with seromas of subcutaneous cellular tissue at different ways of their sanation. Optimal way for treatment of seromas after the alloplasty of incisional hernias is puncture. It shows up in quicker disappearance of extravasate, minimal risk of contamination, of seroma cavity and more favorable and short-term, restorative period.
Key words: seroma, polypropylene reticular prosthetic device, early postoperative period
Хирургическое лечение больных с послеоперационными вентральными грыжами находится в ряду самых важных проблем абдоминальной, реконструктивной и пластической хирургии [4, 6, 9]. Развитие современной герниологии невозможно без применения синтетических материалов для пластики передней брюшной стенки. Более чем 20-летний опыт их использования показал высокую эффективность в восстановлении целостности передней брюшной стенки, особенно при гигантских и рецидивных грыжах. Наиболее прогрессивным, безопасным и изученным материалом считается полипропилен [8].
Грыжесечение, как любая операция, сопровождается значительным повреждением тканей — альтерацией, что патогенетически является первой стадией воспаления. Рассечение и отслойка тканей приводят к открытию огромного лимфатического коллектора, мелких кровеносных сосудов, поэтому в любом случае на раневую поверхность происходит излитие лимфы, крови, развивается серозное воспаление как следующая стадия воспалительного процесса — экссудация. Соответственно, мы имеем дело с хирургической неизбежностью, требующей поиска способов устранения этих нежелательных последствий, для того чтобы далее процесс шел в сторону пролиферации тканей, а не в стадию инфицирования и гнойного воспаления, поскольку изливающаяся секвестрированная жидкость является хорошей средой для развития инфекции [2].
Серомы, или скопления экстравазально расположенного экссудата в подкожной клетчатке, являются самым распространенным осложнением течения послеоперационного периода и встречаются в широких пределах от 0,8 % [5] или 7,1 % [10] до 60 % [1]. Это связано с тем, что некоторые авторы относят серомы не к осложнениям, а к особенностям течения раневого процесса в условиях нахождения инородного материала [2]. В подавляющем большинстве случаев серома образуется при пластике «onlay» [3, 11], причем так называемые острые серомы — скопление жидкости в сроки до 1 месяца — у ряда авторов регистрировались в положении onlay до 95 %. А хронические серомы, сохранявшиеся в среднем до 57 суток, встречались у 74 % пациентов с таким видом пластики [7]. Некоторые авторы считают, что при подапоневротиче-ском расположении сетки проблемы хронических сером не существует [7, 12].
Четких критериев ведения больных с серомами также не разработано. Одними авторами активно пропагандируется пункционный способ ведения [3], другими — длительная вакуум-аспирация [1].
Таким образом, исследование, посвященное спорному, с точки зрения понимания течения раневого процесса, накоплению серозной жидкости вокруг сетчатого протеза и методам борьбы с этим явлением, видится нам весьма актуальным.
Цель исследования: проведение сравнительного анализа ближайших результатов лечения
П11 I I I I III IП11 I I I I I I
больных послеоперационными вентральными грыжами, послеоперационный период которых протекал с серомами подкожной клетчатки, при различных способах их санации.
Для изучения протекания раннего послеоперационного периода были проспективно изучены случаи лечения 183 пациентов, оперированных в 2004 — 2010 гг. по поводу послеоперационных вентральных грыж, послеоперационный период которых сопровождался серомами. Все больные (73 мужчины и 112 женщин) — в возрасте 40 — 60 лет, без тяжелой сопутствующей патологии, прошли предоперационное обследование и оперированы в плановом порядке. Средний возраст пациентов составил 54,6 ± 3,6 года. Сопутствующая патология имелась у 131 больного (71,6 %): ИБС — у 65 человек (35,5 %), артериальная гипертензия — у 57 человек (31,1 %), сахарный диабет II типа — у 27 человек (14,8 %), ожирение II — III ст. — у 32 человек (17,5 %). Оценка физического состояния и анестезиологического риска в группах больных оценивалась по шкале ASA (American Society of Anesthesiologists, 1963). Состояние здоровья 62 (33,9 %) пациентов соответствовало II классу, 121 (66,1 %) — III классу по шкале ASA. Длительность анамнеза основного заболевания составила в среднем 5,1 ± 2,2 года. У 98 пациентов (53,6 %), послеоперационная грыжа возникла в течение первого года после операции. У 49 больных (26,8 %) грыжа была рецидивной. В 105 (57,4 %) случаях первичной операцией была холецистэктомия, в 55 (30,1 %) — ушивание перфо-ративной язвы, в 11 (6 %) — лапаротомия по поводу деструктивного панкреатита, в 28 (15,3 %) случаях
— лапаротомии по поводу прочих заболеваний и травм органов брюшной полости. Все грыжи имели срединную локализацию и по классификации J.P. Chevrel, M.A. Rath (1999) укладывались в значение MW3R0-1. Площадь грыжевых ворот (произведение наибольшего значения ширины и длинны дефекта) в среднем составила 205 ± 53 см2. Операция проводилась под общим обезболиванием (эндотрахеальный наркоз). За 40 минут до операции проводили антибактериальную профилактику путем внутривенного введения 1,0 грамма цефазо-лина (Sandoz, Austria). Выполняли грыжесечение, пластику сетчатым протезом («Эсфил-стандарт», Линтекс, Санкт-Петербург) с диаметром мононити 0,12 мм, толщиной протеза 0,5 мм, объемной пористостью 85 %, поверхностной плотностью 62 г/м2. По способу пластики — сетчатый протез устанавливали всем пациентам на апоневроз (положение «onlay»). Протезы фиксировали только аналогичной сетчатому протезу непрерывной полипропиленовой нитью того же производителя.
По способу ведения послеоперационного периода больные методом слепой выборки (конверты) были разделены на четыре группы:
1) опорожнение серомы через рану с установкой дренажной полоски (применяли на этапах становления методики аллопротезирования) (n = 46);
2) опорожнение через рану без дренажа с ежедневным зондированием линии швов и опорожнением полости серомы (л = 43);
3) установка вакуум-дренажа в полость серомы на 3 суток через отдельный прокол, минуя линию швов (л = 43), установка дренажа на 2 — 3-и сутки при выявлении серомы, удаление — на 6 — 8-е сутки при значительном снижении дебита экссудата;
4) пункционное опорожнение сером (л = 51).
После 12 суток при сохранении экссудации
всех больных из любой группы переводили на пункционное опорожнение сером на 21-е, 36-е и 45-е сутки. Исследуемые группы были сопоставимы по полу, возрасту и диаметру грыжевого дефекта. В первые трое суток после операции в зависимости от самочувствия пациентов вводились только ненаркотические анальгетики.
Оценивали: количество и характер раневого отделяемого, сроки активной и остаточной экссудации, результаты бактериологических посевов и сроки стационарного и амбулаторного лечения.
Результаты приведены в виде средних значений с указанием стандартного отклонения. Статистическую обработку проводили с использованием критерия Манна — Уитни для непараметрического распределения.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ОБСУЖДЕНИЕ
Для подсчета количества отделяемого в первых двух группах в качестве повязки использовали гигроскопичные впитывающие салфетки, сохраняющие в себе жидкость в виде геля аналогично современным детским подгузникам. Ежедневно проводили взвешивание и замену салфетки. В первые два дня во всех группах количество экстравазата было практически одинаковым и с тенденцией к увеличению объема жидкости на 2-е сутки (рис. 1). Лидерами по количеству экссудата явились группы с перманентным персистированием инородного тела в ране: группа 1 — дренажная полоска; группа 3 — трубка вакуумного дренажа. В группе 3 с дренажем по Редону количество жидкости даже увеличивалось на 3 — 4-е сутки, в сроки установки дренажа и дольше сохранялось за счет действия вакуума и, очевидно, меньшего всасывания экстравазата. Несмотря на удаление резинового выпускника через 12 суток и перевод на пункционный способ ведения пациентов всех групп, в первой группе серозное отделяемое сецернировалось до
1,5 месяцев у 10,9 % пациентов, что в 5,3 раза больше по сравнению с группой 4.
Суммарные средние потери экстравазата составили в первой группе 1362 мл, во второй — 1180 мл, в третьей — 1516 мл, в четвертой — 1154 мл. Таким образом, в группе с вакуумной аспирацией по Редону потери экссудата на 154 — 362 мл больше по отношению к другим группам, что на 23,9 % больше, чем в четвертой, на 22,2 % — чем во второй и на 11,2 % — чем в первой группе. Мы связываем это с раздражающим действием дополнительного
инородного тела в брюшной стенке и активного движения интерстициальной и внутрисосудистой жидкости под действием вакуума.
Сроками активной экссудации считали 12 суток (50 мл и более), далее считали экссудацию неактивной, остаточной и не требующей ежедневного опорожнения. При количестве экссудата менее 5 мл пункции полностью прекращали. К концу стационарного пребывания, на 12-е сутки, количество сером в четвертой группе было на 27,2 % меньше чем в первой, на 25,1 % — чем во второй и на 11,1 % — чем в третьей группе (табл. 1). На 45-е сутки количество сером также было минимально только в четвертой группе и составило 1,9 %, что на 9 % меньше, чем в первой группе, на 2,8 % — чем во второй, на 7,4 % — чем в третьей. Максимальный срок полной ликвидации сером в группе 1 составил 65 суток, в группе 2 — 49 суток, в группе 3 — 51 сутки, в группе 4 — 53 суток.
Макроскопически раневой секрет представлял из себя серозно-геморрагическую жидкость в первые сутки с дальнейшим переходом в серозный характер. Микроскопически в первые сутки преоб-
ладали эритроциты, далее в обеих группах их количество прогрессивно сокращалось. В течение трех суток, динамика снижения количества лейкоцитов в первой группе составила от 1,0 ± 0,2 х 109/л до
2,5 ± 0,7 х 109/л; в группе 2 — от 0,9 ± 0,2 х 109/л до 1,8 ± 0,4 х 109/л. Достоверной разницы в клеточном составе экстравазата не обнаружено.
Посев микрофлоры проводился на 4-е сутки послеоперационного периода, доставлялся и оценивался в условиях баклаборатории. Высевание в группе 1 составило 19 случаев (41,3 %), в группе
2 — 15 случаев (34,9 %), в группе 3 — 5 случаев (11,6 %), в группе 4 — 1 случай (1,9 %). В среднем по всем группам микробное присутствие выявлено в 20,8 % случаев сером. По характеру высеваемых микробов выявлена следующая картина. Наиболее распространенным возбудителем являлся Staphylococcus aureus (36,8 %). Остальной спектр микроорганизмов был представлен Staphylococcus spp., Acinetobacter baumannii, Proteus vulgaris, Cory-nebacterium spp., Streptococcus spp. В 7,9 % случаев выделены ассоциации бактерий (Staphylococcus spp., Corynebacterium spp.).
1 сут. 2 сут. Зсут. 4 сут. 5 сут. 6 сут. 7 сут. 9 сут. 12 сут.
Рис. 1. Сроки и объем активной эксудации (М ± о): * — данные достоверны по отношению к остальным группам ф
источник
Еще несколько лет тому назад казалось, что проблема хирургического лечения грыж брюшной стенки решена. Пластика собственными тканями, выполняемая под местной или региональной анестезией, давала хорошие результаты с нулевой летальностью и низким процентом осложнений. Однако, по данным ВОЗ, это справедливо лишь для простых грыж. В сложных случаях, к которым относят прямые и двухсторонние паховые, послеоперационные вентральные и любые рецидивные грыжи, результаты значительно хуже. Так, при прямых паховых грыжах процент рецидива достигает 10, а вероятность повторного рецидива составляет 40% (для послеоперационных — до 50%). Эта статистика стала серьезным вызовом хирургам, оперирующим грыжи брюшной стенки используя собственные ткани, так называемым «натяжным методом».
Многие годы причиной неудач в лечении сложных грыж считали технические просчеты хирурга, неверный выбор варианта операции, сопоставление неоднородных тканей и т.д. Естественный вывод из накопленного опыта – причина рецидива заболевания в другом: в несостоятельности собственных тканей передней брюшной стенки, применяемых для герниопластики.
Закрыть грыжевой дефект без натяжения можно используя синтетический эндопротез. Нами накоплен значительный опыт использовании сетчатых эндопротезов в лечении паховых грыж, которым мы хотим поделиться с хирургами.
Использование синтетических эндопротезов при герниопластике
Потребность в использовании протеза для пластики паховых грыж была признана еще в XIX столетии. Были испытаны различные материалы, включая собственные ткани пациента. К сожалению, выяснилось, что при использовании собственных тканей со временем фасции ослабевает, а при инфицировании — отторгаются. Многие годы были потрачены на поиск материала, не вызывающего отторжения, нагноения и других осложнений.
Были разработаны требования, которым должен отвечать материал идеального эндопротеза:
водопроницаемость и прорастаемость тканями организма
достаточная прочность к внутрибрюшному давлению или внешнему воздействию
стимулирование прорастания фибробластами (в противовес реакции отторжения или секвестрации)
не вызывать реакции воспаления или отторжения
трансформация в нужную форму
способность волокон не запутываться и не разъединяться
не вызывать аллергию или гиперсенсебилизацию
отсутствие канцерогенных свойств
не ощущаться пациентом в качестве инородного тела (быть достаточно жестким и твердым)
не изменять физические свойства под воздействием тканевой жидкости
Фиксация сетки может проводиться как с использованием аналогичной по химическому составу нити, так и специальных автоматических аппаратов (степлеров). Механизация фиксации имплантатов позволяет значительно упростить и ускорить этап реконструкции пахового канала. Кроме того при проведении пластики пахового канала возможно применение полимерных сеток не требующих их непосредственной фиксации. Этот эффект достигается за счет увеличения толщины и веса имплантата (Herniamesh) или введения в состав сетки химических веществ, образующих физико-химическое сцепление с тканями (Sofradim) , так называемые «липучки».
I тип: полностью макропористые монофиламентные полипропиленовые протезы (Линтекс, Prolene, Atrium, Marlex, Surgipro и Trelex). Эти сетки имеют поры размером более 75 микрон, что является необходимым условием для проникновения макрофагов, фибробластов, кровеносных сосудов и коллагеновых волокон в поры и устойчивости к инфицированию. Данный тип материалов вызывает активный ангиогенез и выраженную реакцию фибробластов и служит каркасом для прорастания соединительной тканью, с формированием надежного «протезного» апоневроза. Достаточная молекулярная проницаемость позволяет белковоподобным веществам реципиента проникать в поры, в результате чего происходит быстрая фибринозная фиксация сетки к тканям, что уменьшает риск образования серомы, так как быстро исчезает «мертвое пространство» между сеткой и тканями. При нагноении послеоперационной раны нет необходимости в удалении такого протеза.
II тип: полностью микропористые протезы (расширенный политетрафторэтилен Gore-Tex) с размером пор менее 10 микрон. Микропористые материалы допускают по падание бактерий в поры и исключают проникновение макрофагов, поэтому при их использовании увеличивается риск инфицирования. Данный тип протезов не вызывает достаточно интенсивной пролиферативной реакции и васкуляризации, что приводит не к прорастанию сетки соединительной тканью, а к инкапсуляции. При этом формируется менее плотный рубец по сравнению с первым типом материалов.
III тип: макропористые протезы с мультифиламентными или микропористыми компонентами (политетрафторэтилен Teflon, Surgipro multifilament, Mersilene и Мусго-Mesh). Недостатком этой группы материалов является сравнительно легкая подверженность инфицированию, что связано с присутствием мультифиламентных и микропористых компонентов, которые укрывают бактерии. Также отмечена более выраженная реакция на инородное тело в сравнении с 1 типом материалов.
IV тип: композитные протезы с разными по своим свойствам поверхностями (Parietex Composite, Gore-Tex DualMesh, Europlak). Они предназначены для интраперитонеальной имплантации, так как не вызывают спаечного процесса в брюшной полости.
V тип: жесткие макропористые монофиламентные сетчатые полипропиленовые протезы «Herniamesh». Данный вид сеток в результате особой термической и механической обработки обладают свойствами, необходимыми для бесшовной имплантации.
Общие принципы имплантации протезов
Разработаны и общие принципы имплантации протезов, которые включают в себя следующие моменты:
Для предотвращения образования сером при имплантации необходимо избегать прямого контакта протеза с подкожно-жировой клетчаткой.
Протез должен располагаться между мышечно-апоневротическими тканями, чтобы предотвратить его смещение при повышении внутрибрюшного давления.
Протез должен быть достаточных размеров, чтобы перекрывать края грыжевых ворот на 2-4 см при пластике паховых грыж и на 6-8см при послеоперационных грыжах. Это необходимо для равномерного распределения внутрибрюшного давления по всей площади имплантата. В противном случае, при использовании протеза недостаточных размеров, закрывающего только лишь грыжевые ворота, внутрибрюшное давление будет воздействовать на гораздо меньшую площадь, что приведет к повышению нагрузки по линии швов.
Всегда необходимо фиксировать протез по периферии для предотвращения его сморщивания и смещения. После фиксации к тканям протез должен лежать относительно свободно, со складками и без натяжения, что в свою очередь будет компенсировать повышения внутрибрюшного давления при физической активности пациента и уменьшение размеров имплантата в результате формирования рубца.
Необходимо избегать прямого контакта протезов, изготовленных из нерассасывающихся материалов, с висцеральной брюшиной для предотвращения развития спаечного процесса в брюшной полости, спаечной непроходимости кишечника, врастания сетки в органы и формирования кишечных свищей.
Следует применять с профилактической целью антибиотики широкого спектра действия во время операций по поводу рецидивных и послеоперационных грыж, при использовании больших по размерам протезов, а также при дренировании послеоперационной раны.
Собственный опыт выполнения безнатяжной герниопластики
В клинической больнице 122 им. Л.Г.Соколова с 1998 года прооперированы 1905 пациентов с различной локализацией грыж. По поводу паховых грыж оперированы 1153 больных. В подавляющем большинстве мы использовали способ Лихтенштейна в нашей модификации.
По нашему мнению преимуществами операции с пластикой пахового канала по методике Лихтенштейна являются: редкое возникновение рецидива грыжи — отмечается только у 1,3% пациентов, быстрое выздоровление, низкая степень дискомфорта после операции.
Раневая инфекция. Многие годы считалось, что использование сеток увеличивает риск развития раневой инфекции. По нашему мнению для профилактики раневой инфекции рекомендуем однократное внутривенное введение антибиотика во время операции, что позволило до минимума свести число таких осложнений.
Серома — скопление серозной жидкости в хирургической ране в зоне «мертвого пространства», остающегося в тканях после ушивания. Серомы формируются и после обычной герниопластики, но чаще после использования сетки, как реакция на травму и инородное тело. Как правило, серома появляется на 3 или 4 день после оперативного вмешательства. В зоне операции появляется опухолевидное выпячивание без признаков воспаления. УЗИ позволяет четко локализовть скопление жидкости и определить ее объем. При объеме серомы до 50 мл ведение консервативное, при большем объеме выполняем пункцию и эвакуацию серомы под контролем УЗИ.
Гематома. Это осложнение наблюдали у 0,5%. Развитие напряженной гематомы требует санации раны, путем ее вскрытия и дренирования. Кровоизлияния могут наблюдаться на значительном расстоянии от раны, например, на противоположной стороне.
Невралгия. Это осложнение в той или иной степени наблюдали у 2,2% пациентов, перенесших грыжесечение, в виде болей, парастезии, гиперстезии на сроках до 3 месяцев после операции. Во всех случаях консервативная терапия давала хороший эффект и повторная операция не потребовалась.
Способ использования Parietene ProGrip при лечении паховых грыж
В последние 2 года мы стали при герниопластике успешно использовать сетчатые импланты, в состав которых введены химических вещества, образующие физико-химическое сцепление с тканями (Sofradim) — так называемые «липучки». Мы использовали сетки Parietene ProGrip. Имплантация сетки без пришивания обеспечивает отсутствие натяжения и оптимальные условия для заживления раны, так как при наложении швов может возникнуть неравномерное натяжение тканей с последующими послеоперационными осложнениями: боль, сворачивание сетки, образование «мёртвого» пространства вокруг пришитой сетки, скопление жидкости, долгое заживление и риск развития инфекции.
Применение самоклеющейся сетчатых имплантов позволило уменьшить количество послеоперационных осложнений, упростить и ускорить выполнение операции.
Современная герниология идет по пути увеличения надежности применяемых способов пластики пахового канала с использованием синтетических эндопротезов при одновременном уменьшении травматичности методик. Ранее применявшиеся способы пластики собственными тканями теряют свои позиции. Они быстро вытесняются вариантами пластики «без натяжения», которые продемонстрировали большую эффективность при длительном наблюдении. Использование синтетических эндопротезов позволяет снизить процент рецидива грыжи и восстановить трудоспособность пациента больного в сжатые сроки. В настоящее время по эффективности с ними могут конкурировать только лапароскопические методики.
В нашей клинике работают специалисты, имеющие огромный опыт лечения грыж и использующие как традиционные, так и лапароскопические способы операций. Разработанные показания для использования эти методик позволило существенно улучшить результаты лечения.
Стоимость лапароскопической герниопластики. Стоимость лечения паховой или бедренной грыжи.
Часто мы слышим вопрос: Сколько стоит лечение паховой грыжи? Сколько стоит лечение бедренной или вентральной грыжи?
Вопрос о стоимости лечения, стоимости операции является достаточно актуальным. Нужно учитывать, какие услуги могут быть включены в оплату. Кроме того, затраты на лечение могут варьироваться в зависимости от индивидуального случая. Тем не менее существуют усредненные ориентиры.
Стоимость лечения обычно включает комфортные условия пребывания, а также расходные материалы и дополнительные диагностические процедуры.
При этом Вы будете уверены, что Вам установлен высококачественный имплант с использованием современных технологий.
источник