В медицинской практике грыжа передней брюшной стенки является распространенным заболеванием. Внутренние органы выходят из замкнутого пространства через ослабленные участки. Патология может не доставлять существенного дискомфорта, но последствия приводят к летальному исходу. Этот тип грыж подлежит обязательному удалению.
Под грыжевым выпячиванием понимают выход брюшины с внутренностями через дефект передней стенки. Строение брюшной стенки таково, что некоторые «слабые мест» могут стать грыжевыми воротами – это паховое кольцо и медиальная паховая яма. Со временем грыжевой мешок может опуститься в мошонку или большую половую губу.
Образование патологии (классификация)
В зависимости от места локализации различают следующие виды патологии:
-
паховая – выпячивание семенного канала, петли кишечника, яичника, мочевого пузыря; промежностная – в области тазового дна, выступает в промежностную яму, внешнюю половую губу, прямую кишку; бедренная – развивается у женщин после 30 лет, внутрь может попасть сальник или петля кишечника; пупочная – внутренности выходят из пупочного кольца; белой линии живота – выпирание через щель на средней линии; спигелиевой линии – выпячивание внутренних органов в район прямой мышцы влагалища; вентральные в месте хирургического вмешательства.
Грыжа никогда не может быть безопасной. Дыра в мягком скелете (брюшинной стенке) приводит к осложнениям. Самое опасное – ущемление грыжевого мешка в кольце. Если в нем оказались жизненно важные органы, то дорога каждая минута. Не во всех случаях хирургическая операция полностью решает проблему – часто орган оказывается нежизнеспособным и его приходится удалять.
Не стоит игнорировать грыжу c риском ущемления. Грыжевое кольцо имеет склонность к росту и «затягивает» все больше органов (сальники, кишечник, желудок), что приводит к ее разрастанию. Это полностью исключает возможность вправления и усложняет лечение.
-
вправляемая – может быть вправленной, при нажатии болевой синдром не возникает; не вправляемая – нет возможности вернуть содержимое на свое место, вызывает боль; ущемленная — часть кишки выходит за стенки живота и возникает сдавливание сосудов, что нарушает питание тканей и провоцирует их отмирание.
Пупочная грыжа развивается из-за неправильно развития мышц. Появляется она в первые месяцы у детей, чаще у девочек. Внутрибрюшное давление при плаче или вздутии живота приводит к расширению кольца, куда выпадает кишка.
У взрослых повышенный риск развития патологии появляется после 50 лет. Многочисленные роды, ожирения приводят к ослаблению мышц пресса.
Увеличение внутрибрюшного давления происходит по следующим причинам:
-
постоянный кашель; асцит из-за проблем с сердцем, почками, печенкой; перитонеальный диализ; потеря веса; проблемы с мочеиспусканием, запоры; травмирование.
Послеоперационные грыжи возникают вследствие хирургического вмешательства, когда врач плохо соединил место разреза. Также причинами могут стать воспалительные реакции в ране, длительное применение тампонады и дренирования.
Основной признак грыжи – выпячивание за брюшной стенкой. Первое время оно небольшое и легко вправляется, но может появиться чувство распирания и дискомфорт в этой области. Образование увеличивается при повышении внутреннего давления (кашель, дефекация). Болевой синдром увеличивается после физических нагрузок и приема пищи.
Осложнения развиваются при попадании сальника или части кишки. Происходит ущемление органа, особенно при увеличении давления. Развивается сильная боль, рвота, кишечная непроходимость, повышение температуры и другие признаки интоксикации. При отсутствии операции развивается перитонит и высокий риск смерти.
При пупочной грыже размер кольца не превышает 10 см, но само выпячивание может быть большим. Появляется ущемление, кишечная непроходимость и застой каловых масс.
Грыжа белой линии живота начинается с проникновения жировой клетчатки. Но отличительной особенностью будет резкая боль вверху живота, схожая с приступом язвенной болезни или холецистита.
Опухолевидное образование в паху, по белой линии живота, на месте рубца или около пупка должны стать поводом посещения хирурга. Только врач способен определить правильно диагноз, характер грыжи и способ лечения.
Определить наличие патологии можно при обычной осмотре и пальпации. Обязательно проверяют ЖКТ, печень, мочевой пузырь и грудную клетку. Кишечную непроходимость диагностируют при помощи рентгенографии или КТ. Для определения точной локализации могут использовать барий.
Грыжу диагностируют при визуальном осмотре
При возникновении сомнений врач вводит палец в межгрыжевый канал и просит пациента покашлять. Толчок в этот момент будет свидетельствовать о наличии грыжи.
УЗИ может выявить воспаления в тканях, которые сопровождаются образованием спаечных процессов внутренних органов. Это вызывает опасные осложнения и усложняет лечение.
Исследование проводится в вертикальном положении для определения истончения тканей в районе грыжевых ворот. В более сложных случаях в грыжевом мешке буде обнаружены некоторые органы.
Ультразвуковое исследование помогает исключить другие заболевания со схожей симптоматикой – онкологию, язвенную болезнь, холецистит. Данные помогут изучить состояние патологии для дальнейшего выбора метода удаления.
Патология характеризуются сложной аномалией, лечение требует наличие определенных знаний в области топографии зоны и современных методик лечения.




Любой тип грыжи лечится только хирургическим вмешательством. Для всех грыж, кроме паховой, используют открытую операцию. Больным под общим наркозом разрезают область локализации патологии, вскрывают грыжевый мешок, а потом вправляют выпавшие органы. Подробные этапы проиллюстрированы ниже. Потом врач ушивает края грыжевого дефекта по определенной технологии. Этот этап является наиболее важным, так как будет определять дальнейшие прогнозы по восстановлению и развитию рецидива. Открытые операции сопровождаются болевым синдромом, рубцами на коже и опасностью инфицирования.
Существуют противопоказания к оперативному вмешательству:
Такие больные носят бандаж и корсет. Однако это временное решение, так как постоянное использование подобных приспособлений приводит к деградации мышц и прогрессированию болезни.
Операции по удалению грыжи практикуют более столетия. В медицинской практике разработано более 400 способов пластики стенок. Однако из-за натяжения сшитых тканей высока вероятность растяжения рубцовой ткани и рецидива заболевания. Последний встречается в 12-20%, точное значение зависит от размера грыжи и вида операции.
Сейчас активно используются новые методики, которые исключают внутреннее натяжение. Для этого используют специальную сетку, вставленную в проекцию грыжевого кольца.
Паховые грыжи можно лечить закрытым методом – лапароскопической герниопластикой. Врач в проколы вводит длинный инструмент для вшивания сетки в проекцию грыжевого дефекта. Она закроет все возможные места выхода.
В последнее время активно внедряется комбинированный способ удаления патологии больших размеров. Больному делают небольшой разрез до 4 см для ушивания наружного пахового мешка. Далее с помощью лапароскопической техники изнутри устанавливается сетка.
После операции у 7% больных наблюдаются осложнения:
Окончательное восстановление происходит через неколько месяцев. Очень важной составляющей послеоперационного периода является реабилитация для профилактики рецидива и осложнений.
Первое время пациенты используют бандаж. Рану изолируют стерильной повязкой, чтобы исключить трения. Начинают ходить на второй день после операции. Обязательно проходят курс антибиотиков, врачи назначают обезболивающие средства.
Выписка происходит через 8-10 дней, когда начинается нормальное затягивание раны. Швы с обычными нитками снимают на десятый день.
Дома дважды в день делают перевязки из стерильной марли и лейкопластыря. Рану обрабатывают зеленкой. Принимать душ можно только через 2 недели.
Для ускорения заживления назначают физиотерапевтические процедуры. Первые 2 месяца нельзя носить более 2 кг и напрягать брюшные мышцы. Занятия спортом откладывают на 3 месяца, в течение которого носят послеоперационный бандаж.
Важно следить за питанием. Оно должно быть щадящим и не вызывать проблемы с ЖКТ:
Полностью исключают консервированные и острые блюда, выпечку. Принимают пищу 5 раз в день небольшими порциями. Мясные блюда лучше готовить на пару, остальное – варить.
Врожденную патологию предупредить невозможно. Однако существует ряд мер по профилактике ущемления. Они также относятся к предотвращению развития грыжи у здоровых людей:
-
контроль веса; много двигаться; правильное питание для исключения запоров; за тяжестями приседать, а не наклоняться; исключить воздействие никотина; своевременная диагностика.
Грыжа передней брюшной стенки не всегда сопровождается болью. Однако игнорирование проблемы приводит к ряду осложнений и летальному исходу. Этот вид патологии должен быть удален хирургическим путем.
источник
Грыжа передней брюшной стенки – это врожденное или приобретенное состояние, при котором происходит выпячивание органов брюшной полости через сформировавшийся дефект. Патология выявляется у 2-5% населения планеты. У каждого пятого пациента грыжа ущемляется, что становится поводом к экстренному хирургическому вмешательству. Лечение преимущественно оперативное. Консервативные методы малоэффективны и способны лишь временно облегчить состояние больного, но не избавить полностью от проблемы.
В клинической практике выделяют две формы грыжи:
- Первичная грыжа, возникшая на фоне дефекта передней брюшной стенки.
- Послеоперационная грыжа, сформировавшаяся после хирургического вмешательства.
- Срединная грыжа (эпигастральная и пупочная).
- Боковая грыжа (поясничная и Спигелиевой линии).
- Малые грыжи – до 2 см.
- Средние грыжи – 2-4 см.
- Большие грыжи – более 4 см.
Ширина грыжевого дефекта – это наибольшее расстояние между ее боковыми краями.
По характеру течения различают:
- Вправимые грыжи – можно вправить консервативными методами.
- Невправимые грыжи – не поддаются коррекции и требуют обязательного хирургического лечения.
В структуре грыжи различают:
- Грыжевые ворота – врожденный или приобретенный дефект мышц и связок передней брюшной стенки.
- Грыжевой мешок – часть брюшины, выпячивающаяся через грыжевые ворота.
- Грыжевое содержимое: любой орган брюшной полости. Чаще встречается сальник и петли тонкой кишки.
- Оболочки грыжевого мешка – слои, покрывающие образование.
Основной признак неосложненной грыжи – это появление пальпируемого выпячивания на передней стенке живота. Это может быть единственным симптомом патологии. Возможно появление сопутствующих признаков:
- Боль в области выпячивания. Чаще встречается при послеоперационной и грыже белой линии живота. Боль усиливается после еды, при физической нагрузке.
- Тошнота, рвота. Отмечается преимущественно при эпигастральной грыже.
Грыжа передней брюшной стенки выявляется при первичном осмотре. Во время пальпации врач может определить фасциальный дефект, предположить его размеры. Точную оценку патологии дает УЗИ. Пациентам с ожирением, большим грыжевым выпячиванием и при рецидиве рекомендуется пройти компьютерную или магнитно-резонансную томографию.
При ущемлении грыжи происходит сдавление ее содержимого в грыжевых воротах. Нарушается кровоснабжение пораженного органа, возникает некроз тканей. Спровоцировать такое осложнение могут следующие факторы:
занятия спортом;
- тяжелая физическая работа;
- подъем тяжестей;
- половая жизнь;
- сильное натуживание во время дефекации;
- сильный кашель.
Признаки ущемленной грыжи:
- сильная внезапная боль в области грыжевого выпячивания;
- тошнота;
- рвота с примесью желчи;
- отсутствие стула и отхождения газов (признак кишечной непроходимости).
Ущемление грыжи – повод для немедленного хирургического лечения.
Грыжа возникает на фоне дефекта мышц и апоневроза брюшной стенки. Выделяют две причины развития такого состояния:
- Ослабление передней брюшной стенки. Несостоятельность мышц и связок может быть врожденной или приобретенной.
- Повышение внутрибрюшного давления. Возникает на фоне различных физиологических и патологических процессов.
Сочетание этих двух факторов ведет к появлению грыжи.
Герниопластика с натяжением тканей. Дефект ушивается за счет тканей апоневроза передней брюшной стенки. Выполняется при небольших грыжах – до 3 см, а также у детей. Восстановительный период после герниопластики с натяжением тканей занимает до 6 недель и протекает болезненно. В послеоперационном периоде высок риск рецидива (до 10%).
- Герниопластика без натяжения тканей. Дефект передней брюшной стенки укрывается синтетическим протезом. Хирург устанавливает «заплатку» из полимерных материалов. Не создается натяжения тканей и снижается риск рецидива болезни (менее 3%). Послеоперационный период протекает легче, восстановление тканей происходит быстрее.
- Принимать лекарственные средства по назначению врача. Практикуется прием анальгетиков для купирования боли, антибактериальных препаратов для профилактики инфекционных осложнений.
- Носить бандаж. Бандаж подбирается индивидуально. Он должен прочно удерживать измененные ткани, но не давить на органы брюшной полости.
- Носить компрессионное белье, особенно людям из группы риска по развитию тромбозов.
- Соблюдать двигательный режим. Физические нагрузки после операции ограничиваются. Нельзя поднимать тяжести, заниматься спортом.
- Следить за работой пищеварительного тракта. При запорах рекомендуется прием слабительных препаратов.
- Соблюдать диету. Нужно отказаться от продуктов, повышающих газообразование и замедляющих перистальтику кишечника. Рекомендуется тщательная механическая обработка пищи, приготовление блюд на пару. Стоит соблюдать дробный режим питания – 5-6 раз в день малыми порциями.
соблюдать диету и избегать запоров.
- носить поддерживающий бандаж.
- не поднимать тяжести.
- не заниматься спортом, тяжелой физической работой.
- ущемление содержимого грыжевого мешка;
- нарушение дефекации вплоть до кишечной непроходимости;
- хронический болевой синдром.
- кровотечение во время операции или после ушивания тканей;
- инфицирование;
- отторжение импланта;
- миграция сетки в брюшную полость;
- формирование кишечных свищей;
- прорезывание швов;
- спаечная болезнь;
- рецидив грыжи.
Рациональное питание: не допускать запоров (см. как избавиться от хронических запоров).
- Двигательная активность. На пользу пойдут любые занятия спортом, укрепляющие мышцы передней стенки живота.
- Своевременное лечение заболеваний пищеварительного тракта, ведущих к повышению внутрибрюшного давления.
- Коррекция веса. Важно не допускать ожирения, избегать строгих диет с резким похудением.
- нестабильная стенокардия и свежий (сроком до 6 мес) инфаркт миокарда;
- сердечно-лёгочная недостаточность II и III степени;
- артериальная гипертензия III стадии;
- не поддающийся коррекции сахарный-диабет;
- цирроз печени в стадии декомпенсации.
- диагностика и коррекция сопутствующих терапевтических заболеваний;
- определение резервов и подготовка сердечно-сосудистой и дыхательной систем к изменению объёма брюшной полости и перемещению внутренних органов;
- диагностика сопутствующей патологии, требующей одномоментной хирургической коррекции;
- подготовка кожи передней брюшной стенки.
- Выполняется из лапароскопического доступа без рассечения покровных тканей.
- Через 3 небольших прокола (диаметром 10 мм и меньше) при помощи специальной аппаратуры в месте формирования грыжи фиксируется синтетическая (чаще полипропиленовая или тефлоновая) сетка.
- Этот способ сложнее технически и дороже, но он предпочтителен при лечении рецидивных, двухсторонних грыж, а также в тех случаях, когда необходимо достичь хорошего косметического эффекта.
- Активизация больного начинается непосредственно после операции.
- При использовании лапароскопического метода обеспечивается кратчайший и практически безболезненный послеоперационный период, раннее восстановление трудоспособности.
- Виды
- Формы
- Признаки
- Диагностика
- Лечение брюшной грыжи
- Профилактика
- Операция брюшной грыжи
- После операции
- эпигастральные;
- пупочные;
- инцизионные;
- грыжи Шпигеля.
- эмбриональная;
- возникшая у ребенка;
- впервые образовавшаяся у взрослого человека.
- постоянный кашель, например, при болезнях легких;
- образование избытка жидкости в полости живота (асцит) в результате опухоли, сердечной, печеночной или почечной недостаточности;
- процедура перитонеального диализа, которая используется для терапии почечной недостаточности и опухолей внутренних органов;
- быстрая потеря веса;
- хронический запор или постоянное затруднение мочеиспускания;
- травма живота;
- беременность;
- ожирение.
- вправляемая: выглядит как «шишка» на коже, безболезненна при нажатии, увеличивается в вертикальном положении, может быть вправлена в полость живота;
- невправляемая: не удается поместить содержимое выпячивания внутрь, или это сопровождается болезненностью.
- воспаление;
- задержка каловых масс — копростаз;
- повреждение (травма);
- злокачественное новообразование кишечника.
- беременность;
- сопутствующие заболевания в стадии компенсации и субкомпенсации (например, стабильная стенокардия, гипертония с умеренным повышением давления, сахарный диабет при нормальном уровне сахара и гликированного гемоглобина);
- аденома простаты.
- поддержание нормального веса;
- здоровое питание и регулярные физические упражнения для предотвращения запоров;
- умение поднимать тяжелые предметы без избыточного напряжения мышц живота, не наклоняясь, а приседая за ними;
- отказ от курения;
- своевременное обращение к врачу и плановая операция.
- последовательное рассечение тканей над образованием;
- выделение грыжевого мешка, образованного стенкой брюшины;
- перемещение кишечника и сальника в полость живота;
- перевязка грыжевого образования в области шейки и его удаление;
- закрытие дефекта (герниопластика).
- по Лексеру: используется при маленьком образовании у детей. Образовавшееся после удаления грыжи отверстие зашивают кисетным швом, проще говоря, стягивают;
- по Сапежко: делают продольный разрез, удаляют грыжу, а затем края сухожильного апоневроза и мышц накладывают друг на друга, создавая двойной слой (дупликатуру) и сшивают;
- по Мейо: делают горизонтальный разрез и удаляют пупок вместе с грыжей (об этом нужно заранее предупредить больного); края накладывают друг на друга и сшивают.
- малая травматичность;
- практическое отсутствие послеоперационных осложнений;
- отсутствие швов, рубцов и шрамов;
- быстрое восстановление после операции;
- безболезненность в послеоперационном периоде;
- возвращение к обычной жизни возможно уже через 5 – 7 дней после вмешательства.
- рецидив заболевания (самое частое осложнение);
- задержка мочи;
- инфекция послеоперационной раны.
- легкие супы, овсяная, пшенная, гречневая каша;
- мясо, рыба, яйца;
- кисломолочные продукты;
- фрукты и овощи, соки, кисели;
- морепродукты.
- пожилой возраст;
- большой размер дефекта стенки живота;
- нагноение раны после операции;
- последующие значительные нагрузки и другие причины повышенного внутрибрюшного давления.
В современной хирургии приоритет отдается лапароскопической герниопластике без натяжения тканей. Врач делает 3-4 небольших прокола в передней брюшной стенке и вводит через них инструмент. Ход операции виден на экране. Эндоскопическими инструментами хирург перемещает органы обратно в брюшную полость и накладывает полимерную сетку на грыжевые ворота.
Открытая герниопластика выполняется при наличии противопоказаний в лапароскопической операции. Доступ к грыжевому мешку хирург получает через разрез тканей. Остальные этапы операции не отличаются от таковых при лапароскопии.
Длительность восстановительного периода зависит от объема операции и выбранного доступа. После лапароскопического вмешательства с использованием полимерных материалов восстановление происходит за 3-4 недели. Реабилитация после герниопластики с применением собственных тканей длится до 6 недель. При открытой пластике грыжи восстановление затягивается до 1,5-2 месяцев.
В послеоперационном периоде рекомендуется:
Соблюдение этих рекомендаций снижает риск развития рецидива и ускоряет выздоровление.
Медикаментозное лечение грыжи не предусмотрено. Если операция противопоказана или пациент отказывается от хирургического лечения, рекомендуется:
Эти меры не позволят избавиться от грыжи, но помогут избежать развития осложнений.
Грыжа передней стенки живота может привести к развитию таких состояний:
Своевременное лечение позволяет избежать развития осложнений, сохранить жизнь и здоровье пациента.
Операция по поводу грыжи также не считается безопасной процедурой и может привести к таким последствиям:
Своевременное и грамотное лечение – лучшая профилактика подобных осложнений.
Не существует методов, позволяющих гарантированно избежать развития болезни. Снизить риск появления грыжи помогут такие рекомендации:
При появлении первых симптомов грыжи нужно обратиться к хирургу. Своевременное выявление патологии позволит избежать развития осложнений.
источник
Устранить грыжу и предотвратить осложнения можно только хирургическим путём. Именно поэтому само по себе наличие наружной брюшной грыжи служит показанием к оперативному лечению при условии отсутствия противопоказаний. Операция при неосложнённой грыже носит в значительной мере профилактический характер, поэтому её риск не должен превышать опасность заболевания. Если это условие невыполнимо, приходится прибегать к консервативному лечению.
Соматический статус ряда больных можно характеризовать как очень пожилые, очень больные и очень полные. Вместе с тем ни один из этих признаков не может служить абсолютным противопоказанием к плановой операции. Применение синтетических эксплантатов и имеющиеся возможности анестезиологического и реанимационного обеспечения существенно расширяют показания к хирургическому лечению грыж.
В настоящее время к основным противопоказаниям к хирургическому лечению больных с наружными брюшными грыжами относят:
Консервативное лечение не преследует цель излечения от грыжи (это возможно только у детей первых недель жизни). Оно призвано устранить некоторые тягостные для пациента симптомы, предотвратить увеличение грыжи и её ущемление. Основу подобного лечения составляет ношение бандажа. В комплекс консервативных мероприятий входит подбор диеты, а при необходимости и медикаментозных средств, направленных на предупреждение запора.
Операцию по поводу грыжи традиционно называют грыжесечением.
Она состоит из двух этапов: собственно грыжесечения, то есть удаления грыжи, и пластики грыжевых ворот. Существует огромное количество вариантов пластического закрытия грыжевых ворот, между тем все они связаны с использованием собственных тканей пациента либо аллотрансплантатов. Их использование открыло новый этап в хирургическом лечении грыж — разработке методов ненатяжной герниопластики, которая расширяет возможности хирурга в лечении наиболее тяжёлого контингента больных и существенно снижает частоту рецидивов.
Проведение предоперационной подготовки большинству пациентов с грыжами небольших размеров не требуется, что связано с малым объёмом грыжевого образования, отсутствием редукции объёма брюшной полости и малой агрессивностью самого оперативного вмешательства.
Предоперационную подготовку пациентов с грыжами брюшной стенки больших размеров проводят по следующим направлениям:
Диагностику сопутствующих терапевтических и хирургических заболеваний и их коррекцию проводят в соответствии с общепринятыми канонами, как и перед другими хирургическими вмешательствами. Возраст больного не имеет решающего значения для принятия решения о необходимости оперативного вмешательства. Однако у больных старших возрастных групп с обширными и гигантскими грыжами оно должно приниматься с большей осторожностью.
Учитывая уменьшение объёма брюшной полости пациентов при проведении пластики передней брюшной стенки, особое внимание уделяется функциональному состоянию дыхательной системы. В связи с этим в комплекс обязательного предоперационного обследования пациентов включают изучение показателей функции внешнего дыхания. Нарушения функции внешнего дыхания по обструктивному типу, как правило, связаны с такими заболеваниями лёгких, как хронический бронхит и бронхиальная астма, и требуют терапевтической коррекции. Тем не менее у пациентов с большими вентральными грыжами наиболее часто диагностируют нарушения функции внешнего дыхания по рестриктивному или смешанному типу. Это связано с наличием у пациентов хронических заболеваний, возникающих на фоне грыжевого образования и связанных с гиподинамией и нарушением процессов пищеварения.
Исследование функции внешнего дыхания у всех пациентов с вентральными грыжами проводят как при наличии, так и при отсутствии бандажа. Однако у определённой категории пациентов использовать бандаж не всегда удаётся. Так, его невозможно полноценно применять при невправимых грыжах и явлениях хронической спаечной непроходимости в грыжевом мешке, при гигантских грыжах и грыжах, сформированных вследствие подкожной эвентрации. Всем больным с компенсированным нарушением функции внешнего дыхания в предоперационном периоде показано проведение дыхательной гимнастики, а при значительных и резких изменениях подготовку системы дыхания необходимо проводить в течение 1-2 мес и сочетать с постоянным ношением бандажа.
Нарушения функции кишечника наиболее часто развиваются при наличии спаечного процесса в брюшной полости и грыжевом мешке и невправимой грыже. В связи с этим плановая подготовка кишечника к оперативному вмешательству обязательна. Её применение уменьшает объём содержимого брюшной полости, облегчает выполнение сочетанных операций, служит основой профилактики послеоперационного пареза кишечника и нарушений функции системы дыхания и кровообращения. Подготовка кишечника у пациентов с небольшими грыжевыми образованиями может достигаться постановкой очистительных клизм накануне операции. Однако при больших и гигантских вентральных грыжах предпочтительно назначение многодневной подготовки с использованием бесшлаковой диеты, приёмом вазелинового масла, субтерапевтических доз многокомпонентных растворов типа макрогола (фортранс) и применением очистительных клизм.
Особое значение у пациентов с вентральными грыжами приобретает диагностика требующих коррекции сопутствующих хирургических заболеваний. При их выявлении проводят симультанные хирургические вмешательства. Необходимость их выполнения вызывается тем, что последующее лечение может потребовать разрушения реконструированной передней брюшной стенки. Целесообразно также проводить профилактическую аппендэктомию, так как в последующем операция по поводу острого аппендицита может оказаться технически сложной.
Применение монофиламентных эксплантатов создаёт предпосылки для одномоментного с пластикой брюшной стенки закрытия кишечных и иссечения лигатурных свищей. При выполнении подобных вмешательств особое внимание необходимо уделять подготовке кожи и профилактике раневой инфекции.
При проведении грыжесечения применяют различные способы обезболивания. От их грамотного выбора зависит безопасность выполнения оперативного вмешательства, возможность его расширения, выполнения симультанных операций, применения эндоскопической техники вмешательства, а также применение в амбулаторной практике. Современный арсенал анестезиологических пособий включает местную анестезию (инфильтрационная или проводниковая анестезия), внутривенную многокомпонентную общую анестезию (со спонтанным дыханием или искусственной вентиляцией лёгких) и перидуральную анестезию (в сочетании с внутривенной анестезией или искусственной вентиляцией лёгких).
Местная анестезия.
Наиболее распространённым методом обезболивания при грыжесечении, выполняемом традиционными способами, служит местная инфильтрационная анестезия. По сравнению с общей анестезией она имеет целый ряд преимуществ: пролонгирует в послеоперационном периоде анальгезирующий эффект, обеспечивает раннюю активизацию пациента и не сопровождается тошнотой, рвотой, головными болями и болями в спине. Недостатки её заключаются в трудности тонкой дифференцировки тканей в условиях их инфильтрации и необходимости большего количества времени для достижения эффекта анальгезии после каждого введения анестетика. Основные противопоказания к её применению — ожирение, послеоперационные и рецидивные грыжи, а также выполнение эндоскопических операций.
Эффективность методики местной анестезии во многом определяется психологической готовностью пациента и применением адекватной премедикации. В большинстве случаев оптимально внутримышечное введение пациенту за 1 ч до операции бензодиазепинов (диазепам 0,2-0,3 мг/кг). По показаниям назначают антигистаминные и холинолитические препараты.
При проведении инфильтрационной анестезии традиционно применяют 0,5% растворы новокаина, а при наличии аллергических реакций на новокаин — 1% раствор лидокаина или прилокаина и мепивакаина, а также 0,25% раствор бупивакаина. Лучшее средство для инфильтрационной анестезии — смесь из 1% раствора лидокаина и 0,5% раствора бупивакаина в соотношении 1:1.
Спинальная анестезия.
При проведении хирургических вмешательств у пациентов с паховыми и бедренными грыжами нередко применяют спинальную анестезию. По сравнению с местной анестезией в хирургии паховых грыж она имеет неоспоримые преимущества — полноценное обезболивание, хорошая релаксация мышц, отсутствие инфильтрации тканей области операции анестетиком и длительный обезболивающий эффект. Спинальная анестезия при герниопластике выполняется по традиционной методике с тщательным соблюдением асептики и пункцией субарахноидального пространства на уровне L2-3 или L3-4 в положении пациента на боку. Для её выполнения используют бупивакаин, лидокаин, тетракаин, артикаин и различные фармакологические смеси с эпинефрином (адреналином), фентанилом, морфином и клонидином (клофелином).
Вместе с тем у спинальной анестезии имеется и ряд недостатков. Они заключаются в необходимости специальной подготовки персонала, трудностях применения у пациентов с ожирением и невозможности достаточно ранней активизации больного. В связи с этим спинальную анестезию в основном используют при осложнённых видах паховых грыж и двусторонних операциях. Специфические осложнения — гипотензия, брадикардия, мышечная дрожь, послеоперационная головная боль, общая слабость, тошнота и рвота.
Общее обезболивание в хирургии грыж не имеет принципиальных отличий от анестезии в открытой хирургии. Однако при проведении видеоассистированных и лапароскопических операций следует учитывать создание у пациента пневмоперитонеума и абсорбцию инсуффлируемого углекислого газа. Необходимо отметить, что в хирургии паховых, пупочных и бедренных грыж общая анестезия применяется очень редко, что связано с потенциальным риском её использования. Кроме того, выключение сознания не допускает контакта хирурга с пациентом, а это бывает достаточно важно для выявления небольших грыжевых мешков. В связи с этим применение общей анестезии в хирургии «малых грыж» повсеместно сокращается и ограничивается специальными показаниями, основное место среди которых занимает необходимость выполнения в брюшной полости и верхней половине тела сочетанных с грыжесечением операций. У пациентов с выраженными сопутствующими заболеваниями сердечно-сосудистой и лёгочной систем предпочтение следует отдавать перидуральной анестезии.
Необходимость применения в хирургии грыж синтетических эксплантатов уже ни у кого не вызывает сомнений. Их использование позволяет добиться надёжного закрытия грыжевого дефекта с малым числом осложнений и низкой частотой рецидива заболевания.
Первые попытки применения ауто- и гетеропластических материалов в хирургии грыж заключались в использовании для пластики широкой фасции бедра, лоскутов кожи и мышц передней брюшной стенки, трансплантатов из твёрдой мозговой оболочки и надкостницы. Однако применение этих материалов не обеспечивало необходимой прочности соединительнотканного рубца и надёжного восстановления дефектов передней брюшной стенки, сопровождалось частым нагноением послеоперационной раны, отторжением трансплантата и значительным количеством рецидивов.
Поиск идеальных синтетических материалов для хирургического лечения грыж также прошёл достаточно длинный путь. За всю историю герниопластики предпринимались попытки применения таких имплантатов, как серебряные нити, сетки из тантала и нержавеющей стали, протезов из фортисана, поливиниловой губки, нейлона, силастика, тефлона, углеродистого волокна, полиэстера, полипропилена, политетрафлюороэтилена, полигликолевой кислоты и полиглактина. Большинство из этих материалов после имплантации подвергались гидролизу и биодеградации, не обладали механической прочностью, гибкостью и формоустойчивостью, легко инфицировались и вызывали реакцию отторжения. Некоторые из этих синтетических имплантатов так никогда и не применялись в клинической практике.
Правильный выбор материала для герниопластики имеет ключевое значение для успешного исхода операции. В связи с этим к имплантируемым синтетическим материалам предъявляются определённые требования, соблюдение которых позволяет обеспечить безопасность и надёжность их применения. Идеальный синтетический имплантат должен быть химически инертным, обладать механической прочностью и гибкостью, стимулировать рост фибробластов, а его поры — достаточного для врастания соединительной ткани размера. Кроме того, он не должен вызывать воспаления и отторжения, аллергических реакций и сенсибилизации, а также оказывать канцерогенного воздействия.
Современные синтетические эксплантаты отличаются по толщине, размерам пор, прочности на разрыв, степени жёсткости при сгибании, структуре поверхности и электрическому заряду. Учитывая то, что эти эксплантаты — текстильные изделия, их свойства оценивают стандартными методами контроля текстиля. Для оценки их качества используют американские стандартные методы контроля.
Тест на прочность определяет предел прочности эксплантата на разрыв и отражает реальное состояние сетки, испытывающей прямое действие силы растяжения. Тест проводят методом применения возрастающей нагрузки к узкой полоске материала. Однако, как показывает практика, разрыв имплантата наиболее часто наблюдается в области границы его прикрепления к тканям. В связи с этим, прочность имплантата определяется также и сопротивлением хирургической сетки натяжению швов, которые накладывают на расстоянии 6,5 мм от её края и натягивают с постоянной скоростью до возникновения повреждений имплантата.
Жёсткость имплантата — одно из основных свойств. Для определения жёсткости полоску имплантата помещают над выступающим краем горизонтальной поверхности, в результате чего происходит сгибание волокон полимера под собственным весом. При проведении оценки теста проводят подсчёт длины перекрытия просвета сеткой области выступающей поверхности.
Толщина сетки оказывает прямое влияние на качество результатов пластики; тонкая сетка имеет преимущества. В сочетании с низкой жёсткостью этот параметр имплантата определяет характер сеточно-тканевого взаимодействия, наличие оптимальных показателей которого способствует более быстрому образованию коллагена в области пластики с минимальной вероятностью формирования сером.
Синтетический сетчатый эксплантат — структурный каркас для прорастания соединительной ткани. В связи с этим пористость протеза, определяемая размером отверстий в сетке, — достаточно важный параметр. Оптимальный размер пор сетчатого эксплантата для оптимальной фиксации и прорастания фиброзной тканью должен быть более 50 мкм и превышать среднестатистические размеры фибробласта (15×50 мкм).
Одним из наиболее важных свойств синтетического эксплантата служит его устойчивость к инфекции. Необходимо помнить, что размер большинства бактерий не превышает 1 микрона, размер нейтрофилов и макрофагов составляет около 10 микрон, а размер промежутков известных полифиламентных материалов — менее 10 микрон. В связи с этим в случае развития гнойно-воспалительного процесса после выполнения пластики полифиламентным эксплантатом или политетрафторэтиленовой пластиной (Mersilene, Gore-Tex, Surgipro SPM, Экофлон) возникает необходимость их удаления. При применении монофиламентных имплантатов (Ethicon, Surgipro SPMM, Resorba, Premilene, Braun, Линтекс) даже в случаях формирования абсцесса необходимости удаления сетки при условии адекватного дренирования раны и назначении антибиотиков не возникает.
По своим физико-химическим свойствам синтетические сетчатые эксплантаты, применяемые в хирургии грыж, можно также подразделить на рассасывающиеся и нерассасывающиеся.
Рассасывающиеся эксплантаты — сетки, в состав которых входит полиглактин-910 и полигликолевая кислота. Рассасывание полиглактин-910 эксплантата происходит между 60 и 90-ми сутками после выполнения оперативного вмешательства. Типичные представители эксплантатов, в состав которых входит полиглактин-910, — сетки Vicril, Vypro I и Vypro II (Ethicon). Полигликолевая кислота — синтетический рассасывающийся материал. Полное время его рассасывания превышает показатели полиглактина-910, составляя 90 дней после имплантации. Кроме того, нити полигликолевой кислоты имеют более высокую прочность на разрыв, которая сохраняется в течение 30 дней. Самый распространённый эксплантат, содержащий полигликолевую кислоту, — сетка Ultrapro (Ethicon).
Наиболее популярные нерассасывающиеся материалы — пластины из политетрафторэтилена (Gore Mycromesh, Экофлон), сетки из полиэстера (Mersilene, Sofradim Parietex) и полипропилена (Ethicon, Surgipro, Resorba, Premilene, Braun, Линтекс). Важное свойство полипропиленовых эксплантатов — отсутствие потери их прочности, они не подвергаются гидролизу и биодеградации. Вызывая слабо выраженную воспалительную реакцию, материал способствует образованию соединительной ткани, которая, прорастая в ячейки сетки, практически вовлекает её в толщу формирующегося рубца. Монолитность и гидрофобность мононити обеспечивают имплантату устойчивость к инфицированию. Обширный опыт их применения подтверждает такие качества, как гипоаллергенность, высокую резистентность к инфекции и отсутствие тератогенности.
Политетрафторэтилен — один из распространённых материалов, используемых в герниологии. Пластины из политетрафторэтилена биоинертны и не вызывают спаечного процесса при пористости от 3 до 5 мкм. Полиэстер также широко применяется в качестве пластического материала. Имплантат имеет высокую эластичность, широкие промежутки между волокнами и легко моделируется в ране.
В отдельные категории эксплантатов, применяемых при проведении хирургического лечения грыж, можно выделить композиционные сетки, двусторонние сетки с неадгезивным покрытием и наличием антимикробных компонентов. Композиционные сетки, как правило, состоят из полипропилена и какого-либо гидролизируемого материала. Эксплантаты из рассасывающихся материалов применяются редко, в основном у лиц средних возрастных групп. Основной недостаток таких материалов при закрытии больших грыжевых дефектов — относительно ранняя биодеградация, наступающая до формирования достаточного пласта соединительной ткани. Композиционная сетка состоит из двух типов волокон; она обладает достаточно плотной структурой, обеспечивает механическую прочность и устойчивость к деформации в первые сутки после оперативного вмешательства. В последующем часть волокон подвергается гидролизу, освобождая место для врастающей соединительной ткани. При этом механическая прочность сетки в этот момент времени уже достигается в большей степени за счёт собственной рубцовой ткани.
Наиболее высокотехнологичными синтетическими эксплантатами представляются двусторонние сетки с неадгезивным покрытием (Gore-Tex Dualmesh Plus). Высокую популярность среди хирургов имеют пластины из пористого политетрафторэтилена. Политетрафторэтилен обладает микропористой структурой и способен к растяжению. Он не травмирует ткани, не расслаивается и не осыпается при моделировании, а при пористости менее 5 мкм не прорастает соединительной тканью.
В качестве эксплантатов с наличием антимикробных компонентов необходимо отметить пластины из пористого политетрафлюороэтилена (Экофлон), в состав которых введён дополнительный антимикробный компонент (карбонат серебра или хлоргексидина диацетат). Антимикробный компонент в течение 10 сут высвобождается из структуры пористого материала, тем самым, снижая риск развития раневых гнойно-воспалительных осложнений в зоне герниопластики.
При эндоскопической технике оперативного вмешательства стали применяется сетчатые композитные материалы (Sofradim Parietene), которые также имеют неадгезивное покрытие. Оно представлено коллагеновой плёнкой, которая расположена на одной из сторон полипропиленового сетчатого имплантата и предотвращает развитие спаечного процесса на период его прорастания.
В заключение необходимо отметить, что все применяемые имплантаты в зависимости от их формы можно разделить на плоские сетки и на объёмные. Плоские имплантаты имеют вид прямоугольного листа или же анатомически максимально адаптированных заготовок (Gore-Tex, Herniamesh, Surgipro). Объёмные эксплантаты имеют форму волана или затычки (Bard, Herniamesh, Surgipro), нескольких листов материала, которые могут располагаться в различных плоскостях (Surgipro). Кроме того, в практической работе применяют различные эксплантаты представляющие собой комбинацию плоских и объёмных форм (Herniamesh, Surgipro, Ethicon Prolene Hernia System).
источник
Чем опасны грыжи передней брюшной стенки? Всегда ли нужно ли оперировать бедренные и пупочные грыжи? Как проводится лечение грыж передней брюшной стенки? Можно ли провести операцию при грыже передней брюшной стенки в Европейской клинике установить стенты в толстую кишку?
Своевременное лечение грыж передней брюшной стенки, включая паховые, бедренные, пупочные, белой линии живота, позволяет избежать развития таких серьезных осложнений как острая кишечная непроходимость, повысить качество жизни пациентов.
Грыжи передней брюшной стенки, особенно грыжи белой линии живота, у онкологических больных встречаются как последствия ранее выполненных операций на органах брюшной полости, в результате длительно существующего асцита, а также при слабости соединительной ткани, как и у любых других пациентов, не страдающих раком.
В Европейской клинике работают высококвалифицированные хирурги c большим опытом реконструктивной и эстетической медицины. Использование в нашей клинике современных методик и материалов для пластики грыжи, своевременность проведенного хирургического вмешательства позволяет минимизировать количество осложнений, свести к минимуму рецидивы и обеспечить для пациента комфортный послеоперационный период. При помощи современного эндовидеохирургического оборудования хирургическое лечение проводится в соответствии с принципами эстетической и косметической хирургии. Новые методики позволяют проводить сочетанные (симультанные) операции для индивидуального пациента.
Собственно грыжа — выпячивание внутренних органов или их части без нарушения целости кожи и выстилающей полость оболочки. Отверстие, через которое это происходит называется грыжевыми воротами. Анатомическое строение передней брюшной стенки таково, что существует несколько «слабых» мест, особенностями своего строения предраспололоженных быть грыжевыми воротами. Чаще всего грыжевыми воротами становится паховое кольцо (66% грыж) и соседняя область, называемая медиальной паховой ямкой. Содержимым грыжевого выпячивания в этом случае могут стать тонкая кишка, сальник, изредка слепая кишка, червеобразный отросток, мочевой пузырь, сигмовидная кишка, внутренние женские половые органы. Грыжевой мешок со временем опускается у мужчин — в мошонку, а у женщин — в большую половую губу. Паховые грыжи по расположению грыжевого канала делят на прямые и косые.
Реже встречаются бедренные, пупочные грыжи, грыжи белой линии живота.
Кроме того, выделяют следующие типы грыж — врожденные и приобретенные, травматические, послеоперационные; полные и неполные, вправимые и невправимые, осложненные и неосложненные.
Как правило, пациенты, у которых развиваются грыжи, имеют определенные особенности телосложения и строения соединительной ткани и без того теряющей свою упругость с возрастом. Общее название этих изменений – «синдром слабости соединительной ткани». Современные исследования подтвердили у таких больных нарушения метаболизма коллагена – основного каркасного белка соединительной ткани.
Факторами, способствующими клиническому проявлению грыжи, являются уменьшение (гипотрофия) мышц передней брюшной стенки, повышение внутрибрюшного давления при асците, ожирении, беременности, дискинезии кишечника. Возникновению пупочной грыжи у женщин способствуют многократные беременности и тяжелые роды. Отверстия и щели между мышцами брюшной стенки могут увеличиваться при резком похудании.
Послеоперационные грыжи возникают на месте дефекта ткани, истончения послеоперационного рубца чаще после различных осложнений в области послеоперационного шва (нагноение, инфильтрация и т.п.). У пациентов с онкологическими заболеваниями послеоперационные грыжи могут развиваться на поздних стадиях по факту резкого снижения массы тела, в том числе при развитии раковой кахексии.
Помимо косметического дефекта и дискомфорта, доставляемого грыжей, существует веская причина не откладывать операцию «в долгий ящик». Эта причина – опасность ущемления, т.е. внезапного сдавления содержимого грыжи в грыжевых воротах. Обычно это происходит после поднятия тяжести, сильного натуживания, во время сильного кашля, т.е. при повышении внутрибрюшного давления. Чаще всего ущемляется подвижная тонкая кишка, в ущемленной части кишки нарушается кровообращение, которое через непродолжительное время приводит к некрозу кишки и даже прободению (перфорации) ее стенки с развитием воспаления брюшины (перитонита) – жизнеугрожающего состояния.
Клинически ущемление грыжи сопровождается существенным увеличением грыжевого выпячивания, его невправлением, напряжением и резкой болезненностью. Боли могут локализоваться только в области грыжи или распространяться над всей поверхностью передней брюшной стенки. Поднимается температура, иногда до высокой – 38-39’C. У некоторых пациентов резко снижается артериальное давление с уменьшением систоло-диастолического интервала, например, до 80/60 мм рт.ст. У некоторых пациентов может быть рвота с примесью желчи и даже кала. Развивается острая кишечная непроходимость.
В неосложнённых случаях грыжи обычно достаточно стандартного предоперационного обследования. Диагноз ставится при обычном клиническом осмотре врачом-хирургом. В сомнительных случаях хирург пробует ввести палец в предполагаемый грыжевой канал и просит пациента натужиться или покашлять. При этом ощущается толчок, свидетельствующий о наличии грыжи. Проведение ультразвукового исследования у пациента в вертикальном положении позволяет обнаружить истончение тканей передней брюшной стенки в области грыжевых ворот.
В осложненных случаях в грыжевом мешке при проведении УЗИ можно обнаружить соответствующие органы – кишечник, мочевой пузырь и прочие.
При наличии тошноты, рвоты, болей и отсутствия ущемления органов в грыжевых воротах приходится исключать другие заболевания с подобной симптоматикой. Бывает, что грыжи белой линии живота сопутствуют язвенной болезни, раку желудка, холециститу и др.
Да, всегда. Имеющийся при клинически явной грыже дефект брюшной стенки никакими консервативными мерами или заговорами излечить нельзя. В случае наличия противопоказаний к операции из-за наличия тяжёлых сопутствующих заболеваний пациентам рекомендуется ношение специального бандажа, который несколько замедляет развитие грыжи и препятствует попаданию в грыжевой мешок внутренних органов.
Острые инфекции, беременность на поздних сроках, дерматит и экзема в области грыжи.
Поскольку операция грыжесечения выполняется при общей анестезии, то наличие декомпенсации тяжелых заболеваний внутренних органов, в том числе, ишемической болезни сердца, инсультов, сахарного диабета, является противопоказанием к операции из-за высокой степени анестезиологического риска.
У онкологических больных грыжа передней брюшной стенки лечится по тем же принципам, что и у остальных пациентов.
Оперативное вмешательство, производимое по поводу грыжи называется грыжесечение или герниопластика. Оно заключается в удалении грыжевого мешка, вправлении внутренностей в брюшную полость и укреплении слабого участка брюшной стенки в области грыжевых ворот.
К настоящему времени существует огромное количество модификаций и усовершенствований традиционной герниопластики, поскольку во все времена при этой патологии была велика частота рецидивов — 10% при простых, 30% и более — при сложных видах грыж.
С середины 80-х годов прошлого века предпочтение отдается «ненатяжной» пластике или пластике грыжевого мешка с минимальным использованием собственных тканей. При ненатяжной пластике для закрытия грыжевого дефекта не производится сшивание с натяжением разнородных тканей, а используются синтетические имплантаты. Рецидивов при ненатяжной пластике несравнимо меньше, меньше выражен болевой синдром в послеоперационном периоде, пациент получает возможность выписаться из стационара спустя 2-3 дня после проведенной операции.
При операции герниопластики, проводимой из обычного (открытого) грыжевого доступа, дно грыжевого канала формируется c помощью синтетической сетки. Эта операция технически гораздо проще, чем эндоскопическая, позволяет быстро вернуться к нормальной жизни, обеспечивает значительно менее болезненный и менее продолжительный, чем традиционные операции послеоперационный период. Всего срок послеоперационной реабилитации – 4-5 суток.
Лапароскопическая трансабдоминальная преперитонеальная герниопластика на сегодняшний день признана наиболее обоснованным и малотравматичным вмешательством при паховых и бедренных грыжах.
Хирурги Европейской клиники проводят герниопластику с использованием сетчатых имплантов по поводу паховых, бедренных, пупочных, послеоперационных вентральных грыж. Согласно европейской статистике методики хирургического лечения грыж передней брюшной стенки, применяемые в нашей клинике, позволяют сократить число рецидивов грыжи до 1-2%.
Простая и вместе с тем эффективная методика герниопластики с использованием синтетических материалов обеспечивает пациенту отсутствие болей в послеоперационном периоде, быстрое возвращение к активной жизни, хороший косметический эффект и высокое ее качество в отдаленном послеоперационном периоде.
источник
Одно из самых частых хирургических заболеваний – брюшная грыжа, которая образуется на передней стенке живота.
Грыжей называют выпячивание участка внутреннего органа из замкнутого пространства, например, из брюшной полости. В состав брюшного вида этого образования обычно входит отрезок тонкой или толстой кишки. Она может содержать сальник – это жировой фартук, который отходит от горизонтального отдела толстого кишечника и свисает вниз, прикрывая изнутри стенку живота. Стенка живота включает брюшину, несколько мышечных слоев и кожу. В ней могут образовываться ослабленные участки, через которые выпячиваются брюшные органы.
Грыжа брюшной стенки чаще появляется у женщин, что обусловлено беременностью и более слабыми мышцами живота. Наиболее подвержены этому заболеванию дети дошкольного возраста и люди старше 50 лет.
Содержание:
Брюшная стенка состоит из мышц, расположенных зеркально по обе стороны от средней линии. Это прямые брюшные мышцы, а также поперечные, внутренние и наружные косые. Они соединяются посередине сухожильным образованием – мембраной, или белой линией, ослабление которой приводит к диастазу (расхождению) мышечных групп и формированию грыжи. В этом сухожильном образовании есть отверстия в виде щелей, через которые проникают нервные и сосудистые пучки. Именно здесь чаще возникают грыжевые образования, обычно в верхней трети, реже около пупка или в нижнем отделе живота.
По расположению грыжевого мешка различают такие грыжевые образования:
Эпигастральная грыжа образуется чаще всего у младенцев при ослаблении верхнего отдела средней линии. В этом месте обе прямые мышцы соединяются с нижней частью грудины – мечевидным отростком. Иногда такое грыжевое образование развивается во взрослом возрасте и проявляется выпячиванием в верхней части брюшной стенки.
Пупочная грыжа у взрослого
Пупок – место выхода пуповины, соединяющей в периоде внутриутробного развития плод и материнский организм. После рождения ребенка пуповина отпадает, однако в этом месте остается возможность выхода грыжевого мешка. Грыжа этой области сопровождается выпячиванием пупка. Она часто встречается у младенцев и часто не требует лечения. Необходимость в операции возникает только при появлении неблагоприятных признаков. В дальнейшем оперативное лечение проводится при увеличении размеров грыжи.
Выделяют несколько видов пупочных грыжевых образований:
Эмбриональную форму относят к аномалиям развития, возникающим при нарушении образования полости живота эмбриона. Ее наружная стенка включает пуповинную амниотическую оболочку и недоразвитый листок брюшины.
У детей пупочная грыжа возникает в результате неправильного развития мышц живота. Она чаще образуется у младенцев первых месяцев жизни, преимущественно у девочек. Под действием повышенного внутрибрюшного давления (постоянный плач, запоры, вздутие кишечника) кольцо вокруг пупка расширяется, туда выпячивается часть кишечника. Такие грыжи обычно небольшие.
Во взрослом возрасте такие образования составляют до 5% грыж. Они появляются у людей старше 50 лет, значительно чаще у женщин, после многочисленных родов и на фоне ожирения. Нередко одновременно появляется отвисание живота из-за слабости мышц брюшного пресса.
Инцизионная, или послеоперационная грыжа возникает в результате хирургического вмешательства на органах брюшной полости, если врач недостаточно хорошо соединил ткани после разреза. Однако даже при хорошем ушивании тканей место разреза становится слабее ближайших мышц и потенциально способно стать отверстием для грыжевого содержимого. После лапаротомии грыжевые образования появляются у трети пациентов. Их причинами могут быть воспаление послеоперационной раны, дренирование полости живота и длительное использование тампонады.
Грыжа Шпигеля – редкое образование, возникающее с краю передней брюшной мышцы.
В соответствии со временем появления грыжа живота бывает врожденной и приобретенной. Врожденная форма наблюдается сразу после появления ребенка на свет, приобретенная появляется со временем в ослабленном участке стенки живота. Причиной развития этого заболевания становится высокое давление внутри брюшной полости.
Высокое внутрибрюшное давление возникает в таких случаях:
Вправляемая грыжа: а — под кожу, б,в — вправление вместе с грыжевым мешком
Все эти состояния увеличивают риск приобретенной брюшной грыжи. Существует наследственная предрасположенность к этому заболеванию.
Осложненная форма грыжи – ущемленная. Она сопровождается проникновением части кишки за пределы стенки живота и сдавлением кровеносных сосудов кишки. В результате ткани отмирают и разрушаются, что приводит к болевому синдрому, интоксикации, непроходимости кишечника и перитониту. Ущемление осложняет течения болезни у 20% больных.
Другие осложнения заболевания:
Первое проявление грыжи живота – округлое выпячивание под кожей брюшной стенки. Оно мягкое, безболезненное и вначале легко вправляется при нажатии ладонью. Иногда появляется ощущение распирания, дискомфорта в области основания грыжи. При поднятии тяжестей иногда возникает кратковременная резкая боль. При временном возрастании давления в полости живота, например, при дефекации или кашле, образование увеличивается. Болезненность становится сильнее после приема пищи или нагрузки, нередко возникает запор.
При попадании в грыжевое выпячивание участка кишечника или сальника могут возникнуть признаки осложнений. Орган ущемляется в месте выхода грыжи.Кровеносные сосуды, питающие его, сдавливаются. Это возможно при резком увеличении давления в полости живота. Возникает сильная боль в области грыжи, у больного появляется тошнота, нередко и рвота – признаки интоксикации. Развивается кишечная непроходимость. Она сопровождается вздутием живота, отсутствием стула и газов. Повышается температура тела.
Внезапная резкая боль вверху живота — один из первых симптомов появления брюшной грыжи
Если вовремя не прооперировать больного с таким осложнением, грыжевое содержимое некротизируется, и разовьется перитонит – тяжелое состояние, угрожающее жизни.
У некоторых больных ущемляется только часть кишечной стенки. Явления кишечной непроходимости при этом отсутствуют, выпячивание на животе не увеличивается, однако человека беспокоят нарастающие боли и признаки интоксикации.
Особенность пупочной грыжи – узкие ворота, диаметром не более 10 см. Однако размер самого образования может быть очень большим. Повышается риск ущемления, застоя каловых масс, хронической кишечной непроходимости.
В начальных стадиях грыжи белой линии, когда сквозь ее щели проникает только жировая клетчатка, первым симптомом болезни служит внезапная резкая боль в верхней части живота, напоминающая приступ холецистита или язвенной болезни.
Распознавание грыжи передней брюшной стенки обычно не вызывает затруднений. Она заметна при внешнем осмотре и пальпации живота.
Ущемленная грыжа угрожает жизни, поэтому требуется срочная консультация хирурга. Для диагностики кишечной непроходимости используется обзорная рентгенография живота или компьютерная томография.
Выпячивание, появившееся на передней стенке живота, – повод для обращения к хирургу. Часть кишечника, лежащая в грыжевом мешке, может внезапно ущемится, и при этом потребуется сложная экстренная операция. Срочно обратиться к врачу нужно в случаях появления боли, при внезапном увеличении выпячивания, невозможности вправления, повышении температуры, появлении тошноты и рвоты.
Брюшные грыжи удаляются хирургическим путем. Одновременно восстанавливается целостность мышц живота. Нередко для этого используются синтетические материалы, надежно закрывающие дефект. Цель такого лечения – профилактика ущемления грыжи и развития опасных осложнений.
Если грыжа небольшая, оперативное лечение не требуется. Кроме того, операция не проводится при высоком риске ее осложнений у ослабленных и пожилых больных, а также у пациентов с тяжелыми сопутствующими заболеваниями – тяжелыми нарушениями ритма, выраженной сердечной или дыхательной недостаточностью, злокачественной гипертонией или декомпенсированным сахарным диабетом. Противопоказаниями также являются злокачественные опухоли, острые инфекционные заболевания, обострение воспалительных процессов (пиелонефрита, бронхита, тонзиллита и так далее), гнойничковые заболевания кожи.
К относительным противопоказаниям, при которых операция все же возможна, относятся:
Таким больным предлагаются консервативные способы лечения: бандажи и корсеты. Они считаются лишь временным способом профилактики осложнений и потенциально могут вызвать инфекции кожи из-за постоянного трения. Бандаж можно использовать только при вправимой грыже. Его постоянное применение ослабляет мышцы брюшного пресса и приводит к прогрессированию заболевания.
У 99% детей с пупочной грыжей она не превышает в диаметре 1,5 см и исчезает по мере роста ребенка. Операцию по поводу пупочной грыжи у детей проводят в 3 – 4 года, если к тому времени дефект не исчез. При большом размере грыжи хирургическое вмешательство выполняют, начиная с 1 года жизни ребенка. При небольшом размере образования возможно самоизлечение в возрасте 3 – 6 лет. Однако провести операцию или окончательно отказаться от нее нужно до поступления ребенка в школу. После этого эластичность тканей начинает снижаться, грыжа самостоятельно уже не исчезнет, а размер пупочного кольца будет продолжать увеличиваться.
Врожденные грыжи предотвратить нельзя. Однако следует соблюдать некоторые правила, предотвращающие их ущемление. Эти меры относятся и к здоровым людям для профилактики приобретенного заболевания:
Здоровое питание регулярное питание и занятия спортом — хорошая профилактика запоров
Хирургическое лечение грыж живота проводится под общим наркозом, при небольшом размере выпячивания может использоваться спинномозговая анестезия. Особая подготовка нужна в случае других хронических заболеваний и включает нормализацию давления, уровня сахара в крови и так далее. Также необходима консультация профильного специалиста и заключение о безопасности хирургического вмешательства.
Предоперационная подготовка также требуется при большом образовании. Во время операции перемещение содержимого грыжи в полость живота может привести к внезапному увеличению внутрибрюшного давления, что приведет к нарушению дыхания и кровообращения. Поэтому перед вмешательством используют приемы, направленные на постепенное возрастание давления в полости живота, например, бинтование или бандаж.
Пластику дефекта проводят собственными тканями или синтетическим материалом. Длительность вмешательства составляет около часа.
Основные методы оперативного лечения:
Если грыжа сопровождается диастазом (расхождением) прямых мышц, например, у женщин с ожирением, проводится операция по Напалкову: после удаления образования края сухожилия сшивают, а затем разделяют края прямых мышц с последующим соединением их апоневрозов над белой линией, что укрепляет стенку живота и приводит к уменьшению его объема.
В современных стационарах применяется лапароскопическая методика операции. При этом все манипуляции осуществляются с помощью миниатюрных инструментов, введенных в брюшную полость пациента через небольшие разрезы. Преимущества лапароскопического метода:
Наилучший эффект операции достигается при использовании сетки из полипропилена, реже – из других синтетических материалов. Применяются легкие композитные сетки, через поры которых прорастают волока коллагена, создавая прочную, но упругую ткань, сравнимую с природным апоневрозом. Однако врачи считают применение сеток вынужденной мерой. Эта техника требует от хирурга знаний особенностей этих материалов и хорошего владения техникой операции.
Вопрос о способе закрытия дефекта брюшной стенки решается в каждом случае индивидуально, в зависимости от размеров грыжи и особенностей организма.
Послеоперационные осложнения возникают у 7% больных:
В современных клиниках распространено лечение грыжи в «стационаре одного дня». Операция проводится под местной анестезией, а затем пациента выписывают домой, при условии регулярного врачебного контроля.
Полное восстановление организма после грыжесечения происходит только спустя несколько месяцев после операции. В это время важно пройти последовательные этапы реабилитации, чтобы избежать осложнений и рецидива заболевания.
Сразу после вмешательства больной должен использовать бандаж. На область послеоперационной раны следует класть салфетку из стерильной марли, чтобы предотвратить трение и инфицирование кожи. Вставать и медленно ходить можно уже через день после операции. Назначаются антибиотики и обезболивающие средства.
Пациент выписывается домой через несколько дней, когда врач убедится в нормальном процессе заживления. В домашних условиях необходимо 2 раза в неделю делать перевязки. Используются салфетки из стерильной марли, которые крепятся на кожу лейкопластырем. Края раны можно обрабатывать раствором бриллиантового зеленого.
Бандаж используется пациентом сразу после операции
Если швы были сделаны рассасывающимися нитями, снимать их не нужно. Если же нити обычные, снятие швов проходит на 10-й день в поликлинике. Если рана хорошо зажила, принимать душ можно через 2 недели после вмешательства. В это время назначаются физиотерапевтические процедуры, ускоряющие процесс восстановления.
В течение как минимум 2 месяцев нельзя поднимать предметы весом более 2 кг и делать резкие движения, в том числе напрягать мышцы брюшного пресса. Заниматься физкультурой и спортом не следует в течение 3 месяцев после грыжесечения. В течение 2 месяцев нужно носить послеоперационный бандаж, подкладывая на область шва салфетку из марли.
Питание пациента после удаления грыжи должно быть щадящим, чтобы избежать запоров:
Следует отказаться от острой, соленой, консервированной пищи, алкоголя, свежей выпечки. Есть необходимо 5 раз в день. Готовить пищу следует с использованием оливкового масла, запекать или отваривать. Жарить блюда нельзя.
У большинства пациентов операция очень эффективна. Рецидив грыжи развивается у 10% прооперированных. Факторы риска рецидива:
При развитии ущемления прогноз зависит от объема некротизированной кишки и тяжести интоксикации. В таком случае удаляется часть кишечника, что в дальнейшем приводит к нарушению пищеварения. Поэтому предпочтительнее сделать плановую операцию с низким риском послеоперационных осложнений.
Грыжа живота развивается при выпячивании органов брюшной полости за ее пределы через дефекты в ее стенке. Она бывает эпигастральной, пупочной или послеоперационной. Симптомы заболевания включают выпячивание на стенке живота, чувство распирания и болезненности. При ущемлении возникают симптомы «острого живота». Лечение заболевания оперативное. Для пластики дефекта мышц и сухожилий применяются собственные ткани организма или синтетические сетчатые импланты. При соблюдении техники оперативного вмешательства и восстановительного периода прогноз заболевания благоприятный.
источник
1. Грыжи передней брюшной стенки – пупочные, белой линии живота. Этиология. Клиника. Диагностика. Врачебная тактика. Возрастные показания и способы оперативного лечения.
Грыжа белой линии живота — грыжа живота, выходящая через щель в белой линии живота, расположенной в эпигастральной области или непосредственно над пупком.
Эпидемиология. Грыжи белой линии живота составляют не более 1 % всех видов грыж у детей.
Этиология. Возникновение грыж белой линии живота связано с возникновением поперечных небольших дефектов сухожильных волокон по средней линии, через которые выпячивается предбрюшинная клетчатка.
Клинические проявления. Отмечается округлой формы выпячивание небольших размеров по ходу белой линии живота, расположенное под кожей и не вправляемое в брюшную полость.
Лечение грыжи белой линии живота только оперативное.
Пупочная грыжа — грыжа живота, выходящая через расширенное пупочное кольцо.
Эпидемиология. Пупочные грыжи наблюдаются в 4 % случаев пи отношению к грыжам друтех локализаций
Эмбриогенез. Закрадие пупочного кольца происходит после отпадения пуповины. Наиболее плотно пупочное кольцо закрывается в нижней части, где проходят две пупочные артерии и мочевой проток. Верхний отдел пупочного кольца является слабой зоной, из-за расположения пупочной вены, окруженной рых мой клетчаткой и частого отсутствия здесь пупочной фасции. Верхняя часть ттючного кольца — слабая анатомическая часть передней брюшном стенки, способствует развитию пупочной грыжи.
При внешнем осмотре обнаруживается выпячивание округлой формы в области пупка различных размеров, увеличивающееся при плаче, натуживании.
При пальпации отмечается четкое вправление грыжевого выпячивания в брюшную полость, после чего определяется плотный край пупочного кольца.
Консервативное лечение направлено на спонтанное закрытие пупочного кольца путем комплекса мероприятий, направленных на укрепление мышц передней брюшной стенки.
Хирургическое лечение проводят у детей старше 2-3 лет после неэффективного консервативного лечения и у детей более младшего возраста при грыжах с диаметром пупочного кольца более 2 см,
2. Паховые и ***(И) пахово-мошоночные грыжи в детском возрасте. Этиология. Клиника. Дифференциальная диагностика. Возрастные показания, сроки, способы оперативного лечения. Прогноз репродуктивного здоровья.
Паховая грыжа — грыжа живота, выходящая через наружное кольцо пахового канала.
X. Эпидемиология. Паховые грыжи составляют 90 % среди г рыж разной локализации. У мальчиков они встречаются в 8 10 раз чаше, чем у девочек, и в 2-3 раза чаще справа.
Эмбриогенез. Образование паховой грыжи связано с деоблите- рированным влагалищным отростком брюшины, который появляется на 12-й неделе внутриутробного развития в виде дивертикула брюшины, проникающего во внутреннее кольцо пахового канала. По мере опущения яичка в мошонку влагалищный отросток брюшины опускается вместе с ним, образуя его собственную оболочку. Проксимальная часть влагалищного отростка брюшины после опущения яичка облитериру- ется, и прекращается сообщение между брюшной полостью и мошонкой. Нарушение процесса облитерации влагалищного отростка служит основным фактором развития паховой грыжи.
При внешнем осмотре в паховой области обнаруживается округлой или овальной формы выпячивание, увеличивающееся при плаче, крике ребенка или натуживании и уменьшающееся в спокойном состоянии.
При пальпации определяется эластичной консистенции безболезненное образование, легко вправляемое в брюшную полость с характерным при этом урчанием.
Осложнения. Ущемление паховой грыжи наступает из-за сдавления содержимого грыжевого мешка в грыжевых воротах. Встречается с частотой до 70 % у детей первого года жизни. Сдавление содержимого грыжевого мешка в паховом канале ведет к нарушению венозного и лимфатического оттока из ущемленного органа, к его отеку и еще большему сдавлению. Нарушение артериального притока к ущемленному органу из-за прогрессирующего отека сопровождается его некрозом.
Клинические проявления ущемленной паховой грыжи характеризуются внезапным беспокойством ребенка, плачем, рвотой. Грыжевое выпячивание становится напряженным, резко болезненным и не вправляемым в брюшную полость.
Лечение. Высокая вероятность ущемления паховой грыжи определяет необходимость хирургического лечения независимо от возраста ребенка.
Основная цель хирургического лечения неосложненных паховых грыж состоит в высокой перевязке грыжевого мешка непосредственно на уровне внутреннего пахового кольца.
Ущемленные паховые грыжи с небольшим сроком и без признаков странгуляции возможно вправлять в брюшную полость без операции, что достигается введением седативных и обезболивающих препаратов, использованием теплых ванн и легким массажем грыжевого выпячивания. Если грыжевое содержимое не удается вправить в течение 40-60 мин, что свидетельствует о выраженном отеке ущемленного органа и опасности его странгуляции, то следует ребенка оперировать.
Ущемленные паховые грыжи у девочек подлежат хирургическому лечению независимо от сроков в связи с опасностью некроза яичника, который служит содержимым грыжевого мешка и имеет тенденцию к перекруту.
1 • Рецидив паховой грыжи встречается с частотой не более 1 % при неосложненных грыжах и до 20 % при ущемленных грыжах. Наиболее частые причины щ разрыв истонченного грыжевого мешка у его шейки, соскальзывание лигатуры или ее несостоятельность после перевязки шейки грыжевого мешка, недостаточно высокая перевязка грыжевого мешка.
Повреждение семявыносящего протока составляет до 2 % случаев. Экспериментальные исследования свидетельствуют, что любые инструментальные манипуляции (пинцет, зажим) ведут к последующей окклюзии протока. Семявыносящий проток может быть поврежден при использовании диатермии или при прошивании грыжевого мешка у шейки.
Атрофия яичка после грыжеиссечения встречается с частотой не более 1 %, и она увеличивается до 5 % после хирургического лечения ущемленной паховой грыжи.
Современные технологии в диагностике и лечении паховых грыж. Вероятность наличия паховой грыжи с противоположной стороны составляет 10-15 %. Это обстоятельство послужило основанием для использования УЗИ и лапароскопии в диагностике паховых грыж. УЗИ основано на визуализации необлитерированного влагалищного отростка брюшины. При этом диагностическая точность метода составляет 90 %.
Лапароскопическая диагностика паховой грыжи с противоположной стороны используется во время грыжесечения путем введения лапа роскопа в брюшную полость через грыжевой мешок. Частота необли- терированного влагалищного отростка брюшины с противоположной стороны достигает 32 % и зависит от возраста ребенка. У детей до года она составляет 41 %, на втором году жизни — 37 % и снижается до 19 % у детей старше 10 лет.
Лапароскопическое лечение паховой грыжи рассматривается как альтернативный метод открытому грыжесечению и обладает следующими преимуществами: отличной визуализацией внутреннего пахового кольца и необлитерированного влагалищного отростка брюшины, что позволяет ушить паховое кольцо, не прибегая к дополнительному выделению грыжевого мешка и свести операцию к минимальной трав- матичности. Лапароскопический метод позволяет диагностировать грыжу с противоположной стороны и обеспечивает более благоприятный косметический результат.
3. Синдром портальной гипертензии. Этиопатогенез. Патанатомия. Классификация. Клинические проявления. Методы лабораторной и инструментальной диагностики. Осложнения. Способы консервативного, малоинвазивного, оперативного лечения.
Портальная гипертензия — повышение давления в сосудах бассейна воротной вены выше 200 мм вод.ст.
С патофизиологической точки зрения следует отличать (рис. 5-35) портальную гипертензию, при которой паренхима печени находится под воздействием высокого портального давления (паренхиматозная форма), от портальной гипертензии, при которой высокое портальное давление не оказывает непосредственного воздействия на паренхиму печени (непаренхиматозная форма).
Сопротивление кровотоку в системе воротной вены может локализоваться над, внутри и под печенью. С этой точки зрения все формы портальной гипертензии разделяют на надпечёночную, внутри- печёночную и внепечёночную.
Портальная гипертензия развивается в результате одновременного взаимодействия двух факторов: нарушения оттока венозной крови из системы воротной вены и увеличения притока крови в систему.
При непаренхиматозной портальной гипертензии обструкция току крови расположена до синусоидов печени. Функция печени при этом практически не нарушена, асцит и коагулопатия развиваются очень редко, кровотечение из вен кардии больные переносят относительно легко, а прогноз заболевания в целом хороший. При паренхиматозной портальной гипертензии обструкция току портальной крови расположена позади синусоидов печени. Это приводит к структурному и функциональному их повреждению и ухудшению кровоснабжения гепатоцитов. Вследствие этого нарушается синтетическая функция печени, появляется тенденция к развитию асцита, коагулопатии, труднопереносимым пищеводным кровотечениям и печёночной недостаточности.
Надпечёночная портальная гипертензия
Нарушение венозного оттока от печени (синдром Бадда- Киари, веноокклюзионная болезнь) может возникать в результате порока развития, тромбоза нижней полой или печёночных вен. Портальная гипертензия и нарушение функции печени развиваются вследствие венозного застоя в печени.
Любое хроническое заболевание печени, приводящее к фиброзу или циррозу, может стать причиной внутрипечёночной портальной гипертензии. При большинстве вариантов цирроза узлы регенерации затрудняют отток крови от синусоидов, приводя к пост- синусоидальной обструкции. Наиболее частые причины внутрипечёночной портальной гипертензии — постнекротический цирроз, последствия перенесённого вирусного гепатита, атрезия жёлчных путей, болезнь Уилсона, дефицит альфа-антитрипсина и др. Как правило, развитие портальной гипертензии сопровождается признаками дисфункции печени — желтухой, асцитом, задержкой развития ребёнка и др.
Внепечёночная портальная гипертензия
У подавляющего большинства детей эта форма портальной гипертензии развивается в результате непроходимости воротной вены. Почти у половины детей с внепечёночной портальной гипертензией можно выявить в анамнезе катетеризацию пупочной вены в период новорождённости, омфалит, внутрибрюшные инфекции, сепсис или дегидратацию. Однако у половины детей точный этиологический фактор не может быть выявлен.
Непроходимость воротной вены сопровождается развитием сети коллатералей в воротах печени, получившей название «кавернозной трансформации воротной вены». Такие же венозные колла- терали развиваются вне печени. К ним относят расширенные вены толстой кишки, а также вены, расположенные около селезёнки и в забрюшинном пространстве. По ним кровь из бассейна воротной вены в обход печени возвращается в сердце (рис. 5-36). Наиболее опасны из этих коллатералей варикозно расширенные вены пищевода и желудка. Они становятся причиной рецидивирующих кровотечений.
При врождённом фиброзе печени портальная гипертензия развивается в результате пресинусоидального блока. При этом заболевании портальные тракты увеличиваются за счёт разрастания соединительной ткани и пролиферации жёлчных ходов. При этом типе фиброза синтетическая функция печени остаётся практически неизменной.
У детей чаще встречают внепечёночную форму портальной гипертензии.
Клинические проявления портальной гипертензии в значительной степени однотипны и не зависят от её генеза. Однако при каждом заболевании можно отметить ряд особенностей, помогающих уже клинически выявить форму портальной гипертензии.
Внепечёночная портальная гипертензия
При внепечёночной форме первые симптомы повышения давления в системе воротной вены появляются очень рано. К ним следует отнести увеличение размеров живота, необъяснимую диарею, гипертермию неясного генеза, спленомегалию и появление подкожных кровоизлияний на нижних конечностях. При лабораторном исследовании крови обнаруживают признаки панцитопении со снижением количества эритроцитов, лейкоцитов и тромбоцитов (гиперспле- низм). Внезапное кровотечение из вен пищевода и кардии часто бывает первым проявлением внепечёночной портальной гипертензии у внешне здоровых детей. У 80% больных с внепечёночной портальной гипертензией кровотечения появляются в течение первых 6 лет жизни ребёнка. Изменения функциональных показателей печени обычно незначительны или отсутствуют. Асцит у детей с внепечёночной портальной гипертензией появляется только в первые дни после перенесённого кровотечения.
При внутрипечёночной портальной гипертензии симптомы повышения давления в системе воротной вены наслаиваются на клинические проявления цирроза печени и появляются через 5—7 лет после перенесённого вирусного гепатита. В клинической картине у больных с внутрипечёночной портальной гипертензией на первое место выходят симптомы поражения печени. Больные жалуются на слабость, повышенную утомляемость, похудание, боли в животе, чувство тяжести в эпигастральной области, диспептические явления, повышенную кровоточивость.
Размеры и консистенция печени зависят от стадии заболевания. В начальных стадиях печень умеренно увеличена в размерах, плот ная, поверхность её гладкая. В поздних стадиях заболевания печень обычно не увеличена, нередко даже уменьшена, очень плотная, с буг- ристой поверхностью. В большинстве случаев выявляют увеличение селезёнки различной степени выраженности с развитием признаков
При лабораторных исследованиях обнаруживают нарушение функ- ций печени — гипербилирубинемию с преобладанием прямой фрак- ции билирубина, уменьшение количества белка сыворотки крови со снижением альбумин-глобулинового коэффициента, снижение антитоксической функции печени. Однако изменение этих показателей не всегда идёт параллельно развитию портальной гипертензии, что связано с большими компенсаторными возможностями печени и неспецифичностью так называемых печёночных проб. Проявления внутрипечёночной портальной гипертензии — асцит и кровотечения из вен пищевода и кардии — возникают, как правило, при достижении больным подросткового возраста.
Диагноз портальной гипертензии может быть установлен на ос новании УЗИ брюшной полости и допплерографии висцеральных вен. Характерные признаки внепечёночной портальной гипертензии — кавернозная трансформация воротной вены и нормальная структура печени. При паренхиматозной портальной гипертензии печень уплотнена, воротная вена хорошо проходима. При надпечёночной портальной гипертензии отмечают непроходимость печёночных вен или нижней полой вены. При допплерографии при всех формах портальной гипертензии отмечают значительное снижение средней скорости кровотока в висцеральных венах. Для паренхиматозных форм портальной гипертензии характерен гипердинамический тип висцерального кровообращения.
При ФЭГДС у детей с портальной гипертензией обнаруживают варикозно расширенные вены пищевода и кардиального отдела желудка, а также признаки гипертензионной гастропатии. Вены пищевода и кардии бывают практически единственными источниками кровотечений у детей с портальной гипертензией. Кровотечения из других вен ЖКТ у детей возникают исключительно редко.
В сомнительных случаях или при планировании хирургического лечения необходимо проведение висцеральной ангиографии (рис. 5-37). Дигитальная субтракционная ангиография даёт наиболее полную информацию об анатомии висцеральных вен.
Пункционная биопсия печени показана для определения стадии цирроза или дифференциальной диагностики цирроза печени с другими формами паренхиматозной портальной гипертензии.
Лечение детей с пищеводными кровотечениями в острой стадии включает седативную терапию, введение назогастрального зонда для аспирации желудочного содержимого и инфузионную терапию кри- сталлоидными растворами и препаратами крови в объёме 50% необходимой суточной потребности.
Широкое распространение в настоящее время получила эндоскопическая склеротерапия или эндоскопическое лигирование вен пищевода и кардии.
Основная задача хирургического лечения портальной гипертензии — ликвидация и предотвращение кровотечений из варикозных вен пищевода и желудка. Резко выраженная спленомегалия или выраженный гиперспленизм могут быть отдельными показаниями к манипуляциям на селезёнке. У детей с паренхиматозной портальной гипертензией показанием к хирургическому лечению может быть асцит, резистентный к консервативной терапии.
Современные методы оперативного лечения портальной гипертензии у детей включают выполнение различных портосистемных анастомозов или операций, непосредственно воздействующих на варикозные вены пищевода и желудка.
Методы лечения портальной гипертензии значительно различаются в зависимости от формы заболевания, наличия и выраженности пищеводных кровотечений, а также уровня подготовки специалистов лечебного учреждения, где больной проходит курс лечения. Идеальной для детей с внепечёночной формой портальной гипертензии можно считать операцию мезопортального шунтирования, после которой наряду с нормализацией давления в системе воротной вены происходит восстановление портального кровообращения (рис. 5-38).
Для ликвидации спленомегалии и гиперспленизма в настоящее время используют эндоваскулярную эмболизацию паренхимы органа вместо спленэктомии.
Единственный метод лечения терминальных стадий цирроза печени — трансплантация печени.
4. Кистозные образования (паразитарные и непаразитарные) печени, селезенки, почек. Этиология. Патогенез. Классификация. Клинические проявления. Диагностический скрининг. Современные способы диагностики. Осложнения. Обоснование выбора консервативной тактики: динамическое наблюдение, чрезкожные пункции. Показания к оперативному лечению: эндоскопическому, открытому.
Врожденные кисты печени — кистозное поражение паренхимы и связь печени.
Распространенность врожденных кист печени
По данным аутопсии встречаются в 0,8-1,8% случаев в популяции.
Этиопатогенез врожденных кист печени
Кисты печени образуются вследствие нарушения эмбрионального развития внутридолевых протоков и связочного аппарата печени. Размеры их могут быть от 1-2 мм до 20 см и более. Внутренняя поверхность кист выстлана кубическим или цилиндрическим эпителием (истинные кисты), в их стенке могут быть желчные протоки. Содержимое кист — прозрачная или слегка желтоватая жидкость, реже — желеобразная или коричневая жидкость.
Классификация врожденных кист печени
1. Единичные (солитарные) кисты: a) простые; b) дермоидная; c) ретенционные. 2. Поликистоз (множественные кисты) с поражением: a) только печени; b) в сочетании с поражением почек; c) кисты связь печени. По клиническому течению кисты могут быть: Неосложненные кисты. Осложненные кисты: a) разрыв кисты; b) нагноение кисты; c) с фиброзом печени и портальной гипертензией; d) с печеночной недостаточностью.
Клиника врожденных кист печени
Клиническое течение кист печени чаще бессимптомно. Кисты обнаруживаются случайно при диспансерном обследовании детей с помощью ультразвука. Большие единичные кисты могут сопровождаться следующими симптомами: • Ощущение тяжести после приема пищи. • Боли в правом подреберье. • Увеличение печени с пальпаторно определением опухолеподобных узлов. • В тяжелых случаях — асцит, варикозное расширение вен пищевода, печеночная недостаточность.
Диагностика врожденных кист печени
1. УЗИ печени, органов брюшной полости и почек. При этом в печени обнаруживаются ехонегативни единичные или множественные разных размеров, круглые, наполненные жидкостью полости с фиброзными изменениями паренхимы печени. Однаккистидиаметром 1-4 мм могут не визуализироваться этим методом. 2. Компьютерная томография с уточнением топографической локализации полостей в сегментах печени. 3. Прицельная, под ультразвуковым или рентгеновским контролем, пункция кисты с проведением цистографии. 4. Лапароскопия.
источник
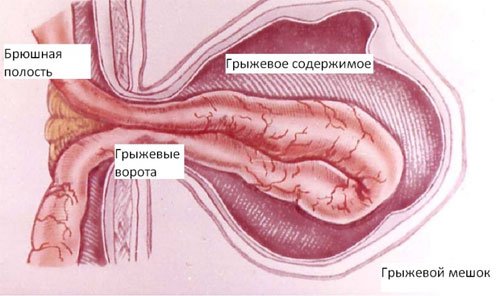
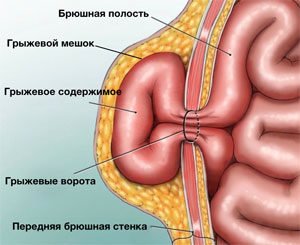
 занятия спортом;
занятия спортом; Герниопластика с натяжением тканей. Дефект ушивается за счет тканей апоневроза передней брюшной стенки. Выполняется при небольших грыжах – до 3 см, а также у детей. Восстановительный период после герниопластики с натяжением тканей занимает до 6 недель и протекает болезненно. В послеоперационном периоде высок риск рецидива (до 10%).
Герниопластика с натяжением тканей. Дефект ушивается за счет тканей апоневроза передней брюшной стенки. Выполняется при небольших грыжах – до 3 см, а также у детей. Восстановительный период после герниопластики с натяжением тканей занимает до 6 недель и протекает болезненно. В послеоперационном периоде высок риск рецидива (до 10%).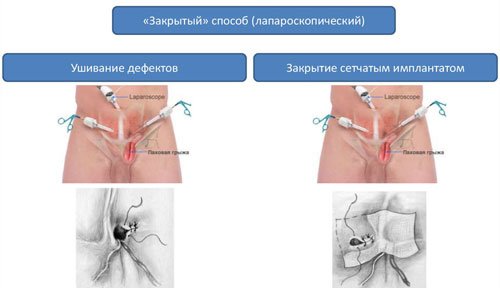
 соблюдать диету и избегать запоров.
соблюдать диету и избегать запоров. Рациональное питание: не допускать запоров (см. как избавиться от хронических запоров).
Рациональное питание: не допускать запоров (см. как избавиться от хронических запоров).